题目内容
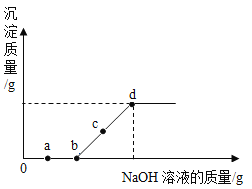
【题目】向某盐酸和氯化镁的混合溶液中加入某浓度的氢氧化钠溶液,产生沉淀的质量与加入氢氧化钠溶液的质量关系量如图所示。请回答下列问题:
(1)a点溶液中滴入紫色石蕊试液,观察到_____。
(2)bc段(不含b点)反应的化学方程式_____。
(3)c点溶液中存在的阳离子为_____。
(4)溶液中NaCl的溶质质量分数d_____c(填“>”“<”或“=”)
(5)d点溶液中的溶质是_____。
【答案】溶液变红色 ![]() 钠离子、镁离子 > 氯化钠
钠离子、镁离子 > 氯化钠
【解析】
解:(1)a点溶液中,稀盐酸部分反应,溶液显酸性,滴入紫色石蕊试液,观察到溶液变红色。
故填:溶液变红色。
(2)bc段(不含b点),氯化镁和氢氧化钠反应生成氢氧化镁沉淀和氯化钠,反应的化学方程式:![]() 。
。
故填:![]() 。
。
(3)c点溶液中存在的阳离子为反应生成氯化钠中的钠离子和没有反应的氯化镁中的镁离子。
故填:钠离子、镁离子。
(4)溶液中NaCl的溶质质量分数d大于c,这是因为d点氯化钠质量继续增大,氯化钠增大的幅度大于溶液质量增大的幅度,因此溶质质量分数增大。
故填:>。
(5)d点溶液中的溶质是氢氧化钠和盐酸、氯化镁完全反应生成的氯化钠。
故填:氯化钠。

练习册系列答案
相关题目