题目内容
【题目】实验室常用加热氯酸钾和二氧化锰混合物的方法制取氧气,请回答下列问题:
(1)用双氧水和二氧化锰制取氧气,反应原理是_____(用化学方程式表示)
实验一般由以下几个步骤:
1.向a仪器中倒入双氧水 2.向b容器中加入少量二氧化锰 3.按要求装配好仪器 4.检查装置的气密性 5.收集气体
其中操作正确的是_____(填下列选项)
A 12345 B 34215 C 34125 D 43215
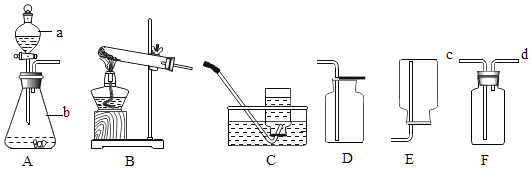
(2)写出下列编号仪器的名称a_____
(3)用所给仪器组装用上述反应制氧气的装置,你选择的发生装置为_____,收集装置为_____(填编号),选择这些装置的依据是_____(填字母)。
A 属于固固型加热的反应 B 属于固液型不加热的反应
C 制取的气体密度比空气大 D 制取的气体难溶于水
(4)若用图F装置进行“排空气法”收集制取的O2,则气体的流向是导气管_____进气_____出气。
(5)若在反应后的残余物中提纯KCl,需进行以下操作,请把空缺处填上:
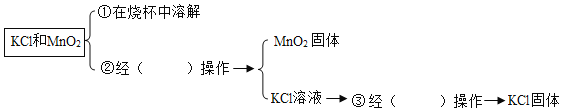
②_____③_____
在①、②、③的操作中均用到的仪器是_____。
(5)若用氯酸钾和二氧化锰制取氧气,收集到的氧气质量为9.6g,理论上需要氯酸钾固体多少摩尔?_____
【答案】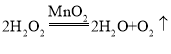 B 分液漏斗 A C或D BCD c d 过滤 蒸发结晶 玻璃棒 0.2mol
B 分液漏斗 A C或D BCD c d 过滤 蒸发结晶 玻璃棒 0.2mol
【解析】
(1)过氧化氢在二氧化锰的催化作用下,受热分解生成水和氧气,反应原理是: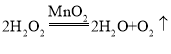 ;用过氧化氢溶液制取氧气,首先将装置连接起来,然后检查装置的气密性,先加固体后加液体,最后收集气体。 故填:
;用过氧化氢溶液制取氧气,首先将装置连接起来,然后检查装置的气密性,先加固体后加液体,最后收集气体。 故填: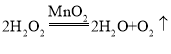 ; B;
; B;
(2)a是分液漏斗,通过分液漏斗可以向锥形瓶中注入液体药品;b是锥形瓶,常用作反应容器。故填:分液漏斗;锥形瓶。
(3)利用过氧化氢在二氧化锰的催化作用下制取氧气,选择“固液装置”,应该用A装置作为发生装置,因为氧气的密度比空气大,可以用向上排空气法收集,可用D装置收集,氧气不易溶于水,可以用排水法收集,可用C装置收集。故填:A,C或D,BCD;
(4)若用图F装置进行“排空气法”收集制取的O2,则气体的流向是“长进短出”,从导气管c进气d出气;故填:c,d;
(5)通过过滤可将难溶于水的固体物质与液体分离,用蒸发结晶法可将溶质从溶液中分离出来,故②是过滤;③是蒸发结晶。①中玻璃棒搅拌可以加快氯化钾的溶解;②中过滤时应该用玻璃棒引流;③中通过用玻璃棒搅拌可以防止液体外溅,因此在①、②、③的操作中均用到的仪器是玻璃棒。故填:②过滤;③蒸发结晶;玻璃棒。
(6)若用氯酸钾和二氧化锰制取氧气,收集到的氧气质量为9.6g,设理论上需要氯酸钾固体质量为x。
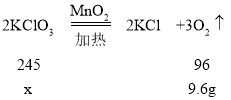
![]() ,解得x=24.5g
,解得x=24.5g
理论上需要氯酸钾固体的摩尔质量为:![]() ×2=0.2mol。故填:0.2mol。
×2=0.2mol。故填:0.2mol。

 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案