题目内容
【题目】金属钨(W)可做白炽灯泡的灯丝。用黑钨矿[主要含有FeWO4(钨酸亚铁)]制得金属钨(W)的工艺流程如图所示:
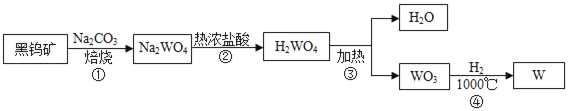
其主要反应原理如下:
①4FeWO4+4Na2CO3+O2![]() 4Na2WO4+2Fe2O3+4CO2
4Na2WO4+2Fe2O3+4CO2
②Na2WO4+2HCl(热浓)=H2WO4+2NaCl
③H2WO4![]() H2O+WO3
H2O+WO3
④3H2+WO3 ![]() W+3H2O
W+3H2O
下列说法不正确的是( )
A. 反应③属于分解反应
B. 反应①②③④的产物都有氧化物
C. 反应①④中有元素的化合价发生改变
D. 为加快反应的速率,可将黑钨矿石碾成粉末
【答案】B
【解析】
A. 反应③中反应物有一种,生成物有两种,属于一变多,属于分解反应,说法正确,不符合题意;
B. ①中的产物![]() 属于氧化物;②中的产物无氧化物;③中产物
属于氧化物;②中的产物无氧化物;③中产物![]() 属于氧化物;④中产物
属于氧化物;④中产物![]() 是氧化物;说法不正确,符合题意;
是氧化物;说法不正确,符合题意;
C. 反应①④中都有单质参加反应,单质中元素的化合价为零,化合物中元素的化合价不为零,故①④中有元素的化合价发生改变,说法正确,不符合题意;
D. 增大物质的表面积可以加快反应速率,为加快反应的速率,可将黑钨矿石碾成粉末,说法正确,不符合题意。故选B。

【题目】水是生命活动中的重要物质.
(1)下表为某品牌营养素饮料标签的部分内容,请根据表中信息回答问题.
营养成分 | 糖类 | 钠 | 钙 | 锌 | 维生素C | 维生素B6 |
含量/500mL | 22.5g | 16mg | 16mg | 3.0mg | 100mg | 0.56mg |
该饮料含有六大营养素中的_____种;该饮料中的_____元素对预防青少年佝偻病有益;该饮料pH为3.5,此饮料呈_____性(填“酸”、“碱”或“中”).
(2)如图为电解水的实验装置,负极产生的气体是_____,该反应的化学方程式为_____.

(3)保护水资源是每个公民应尽的责任和义务.下列防止水污染的措施可行的是_____.
A抑制水中所有动植物生长 B不任意排放工业废水
C禁止使用农药和化肥 D生活污水处理后再排放.
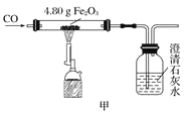
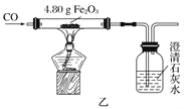
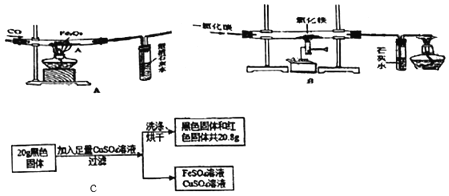
【题目】杨敏在实验室进行CO还原氧化铁的实验采用酒精灯加热(图A)与书本实验(图B)现象相同,发现在得到的黑色粉末中加稀盐酸,没有气泡产生,杨敏就图A实验中反应后得到的黑色粉末的成分进行了如下探究。
(查阅资料)①铁粉及铁的几种常见氧化物的颜色及部分性质。
物质 | 铁粉 | Fe2O3 | Fe3O4 | FeO |
颜色 | 黑色 | 红棕色 | 黑色 | 黑色 |
能否被磁铁吸引 | 能 | 不能 | 能 | 不能 |
②实验室酒精灯的温度为400﹣500℃,酒精喷灯的加热温度在1000℃左右。
③当温度高于300℃以上,Fe2O3容易被还原成Fe3O4;当温度高于600℃以上,Fe3O4容易被还原FeO;当温度高于700℃以上,FeO容易被还原成Fe;
(提出问题)图A实验得到黑色粉末的成分是什么?
(提出猜想)黑色粉末的成分是:①FeO、Fe3O4②FeO③Fe3O4;④FeO、Fe3O4、Fe2O3。
(分析与评价)猜想_____错误,理由是_____。
(1)装置A有一处明显错误,该错误是_____。
(2)请写出澄清石灰水中发生的反应的化学方程式_____。
(3)由对比实验可知,还原氧化铁的实验产物与_____有关。
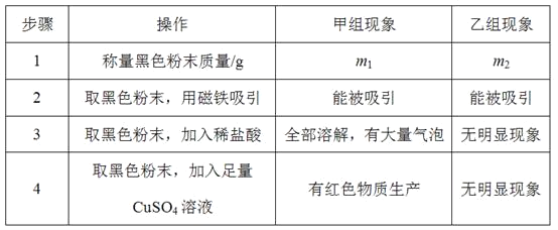
(实验设计)将图A实验得到黑色粉末倒在一表面皿中,用磁铁接触黑色粉末,出现_____现象,说明猜想②正确。
(4)实验B最后得到的黑色固体可能是Fe和Fe3O4,中的一种或两种。小海设计如下实验探究其成分,请帮助他完成该探究过程。
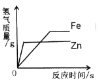
(探究过程)①定性研究:取少量的图B实验得到的黑色粉末于一试管中,加入适量的硫酸铜溶液,充分振荡,出现_____现象,证明黑色固体中有铁。
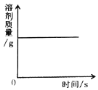
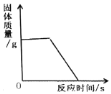
②定量研究:取B实验得到的黑色固体20g,设计如图C实验:试推测黑色固体的成分是_____。
③有同学试图通过反应前后固体质量的变化来确定黑色固体的成分,你认为可行吗?(假设氧化铁在反应中完全反应)_____(填“行”或“不行”)理由是_____。
【题目】中和反应在日常生活中应用广泛,下列是稀盐酸和氢氧化钠溶液反应的微观示意图。回答以下问题:
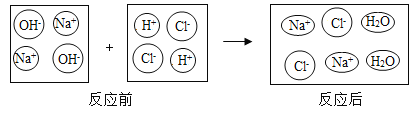
(1)分析图中反应前后没有发生变化的微粒是_____、_____;反应的实质是_____。
(2)如果规定上述反应后溶液的pH<7,显酸性。请你设计一个实验方案证明溶液显酸性:
实验操作 | 实验现象 | 实验结论 |
①______ | ②______ | 显酸性 |
【题目】有一包未知粉末,其中含有碳酸钠、氢氧化钠、碳酸钙、生石灰、氯化钠、硫酸铜六种物质中的四种。兴趣小组为确定其组成设计并进行如下实验。
【实验一】甲组同学进行定性探究。
实验操作 | 实验现象 | 实验结论及分析 |
(1)取少量该未知粉末于烧杯中,加入足量的水溶解、过滤。 | 粉末部分溶解, 得到白色滤渣和无色滤液。 | 原粉末中一定不含_____; 白色滤渣不一定是原粉末中的碳酸钙,其理由是_____(用化学方程式表示)。 |
(2)向滤液中滴加无色酚酞试液。 | 溶液变红 | 滤液中存在碱性物质。 |
(3)向(2)中滴加足量稀盐酸。 |
| 原固体粉末中一定含有Na2CO3。 |
【实验二】乙组同学进行定量探究。
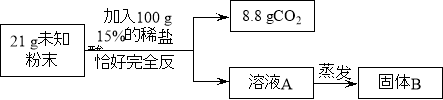
实验测得固体B中含15 g氯元素。试综合甲、乙两组同学的实验进行分析。
(1)乙组实验中一定发生的化学反应是:Na2CO3+ 2HCl=2NaCl + H2O+ CO2↑和 。
(2)该未知粉末的组成可能是 。