题目内容
【题目】人体胃酸(主要成分是盐酸)过多会引起很多胃病,如图为某抗酸药标签上的部分文字,某同学取一片药片,研碎后与质量分数为5%、密度为1.02g/mL的盐酸进行反应,反应的化学方程式为3HCl+Al(OH)3═AlCl3 +3H2O(药片中的其它成分不与盐酸反应),测得反应消耗的盐酸的体积为6.0mL.通过计算,该药片中氢氧化铝的含量_____(填是、否)达标?

【答案】否
【解析】
根据质量=密度×体积,先计算盐酸溶液的质量,再计算盐酸中的溶质质量,最后计算出氢氧化铝的质量。
每片药物消耗的盐酸中含HCl的质量为6.0 mL×1.02g/mL×5%=0.306g
设每片该药物含氢氧化铝质量x。
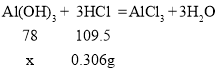
![]()
解之得:x≈0.218g=218mg<250mg
答:该药片中氢氧化铝的含量否达标。

练习册系列答案
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案
相关题目