题目内容
【题目】某化学实验小组在完成实验室制取二氧化碳的实验后,过滤得100g混合溶液,已知其中H+和Ca2+的个数比为1:1,向其中加入20g碳酸钠样品(杂质既不溶于水也不与其他物质反应),恰好完全反应后过滤,得到14.1g滤渣,求所加碳酸钠样品的纯度为( )
A.26.5%B.53%C.79.5%D.84.8%
【答案】C
【解析】
实验室制取二氧化碳的实验后,滤液中含有稀盐酸和氯化钙,向混合溶液中加入碳酸钠样品,稀盐酸先与碳酸钠反应生成氯化钠、二氧化碳和水,氯化钙再和碳酸钠反应生成碳酸钙沉淀和氯化钠,方程式为:![]() ,
,![]() ,由反应方程式可知,每个碳酸钠“分子”和两个氯化氢“分子”反应,和1个氯化钙“分子”反应,又因为H+和Ca2+的个数比为1:1,所以和氯化钙反应的碳酸钠是和盐酸反应的氯化钠质量的2倍,设与盐酸反应的碳酸钠的质量为x,则与氯化钙反应的碳酸钠的质量为2x,生成碳酸钙的质量为y
,由反应方程式可知,每个碳酸钠“分子”和两个氯化氢“分子”反应,和1个氯化钙“分子”反应,又因为H+和Ca2+的个数比为1:1,所以和氯化钙反应的碳酸钠是和盐酸反应的氯化钠质量的2倍,设与盐酸反应的碳酸钠的质量为x,则与氯化钙反应的碳酸钠的质量为2x,生成碳酸钙的质量为y
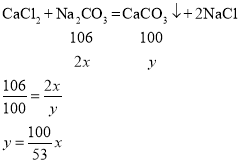
根据题意可知![]() ,则样品中碳酸钠的质量为3x=15.9g,纯度为
,则样品中碳酸钠的质量为3x=15.9g,纯度为![]() ,故选C。
,故选C。

练习册系列答案
相关题目