题目内容
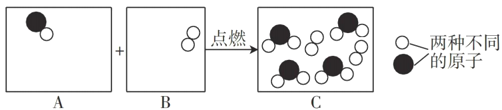
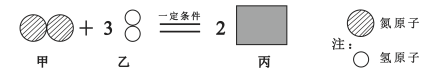
【题目】硝酸铵(NH4NO3)受热可分解为N2、H2O和某种氮的氧化物X.取一定质量的NH4NO3固体充分加热,测得反应后生成N2、H2O、X的质量分别为mg、14.4g、9.2g.下列说法正确的是
A.NH4NO3属于复合肥
B.该反应方程式中N2与H2O的化学计量数之比为1:4
C.X的化学式为NO
D.m=8.4
【答案】D
【解析】
A、氮、磷、钾三种营养元素,含有两种或两种以上的化肥称为复合肥,NH4NO3属于氮肥,A错。
B、根据质量守恒,化学反应前后元素质量不变,故硝酸铵中氢元素质量等于水中氢元素质量,设硝酸铵质量为x,则x×![]() =14.4g×
=14.4g×![]() ,则x=32g,则m=32g-14.4g-9.2g=8.4g,设氮气和水的化学计量数分别为ab,则(a28):(b18)=8.4g:14.4g,故a:b=3:8,故B错。
,则x=32g,则m=32g-14.4g-9.2g=8.4g,设氮气和水的化学计量数分别为ab,则(a28):(b18)=8.4g:14.4g,故a:b=3:8,故B错。
C、根据质量守恒元素质量不变,故X中氮元素质量为,32g×![]() -8.4g=2.8g,X中氧元素质量32g×
-8.4g=2.8g,X中氧元素质量32g×![]() -14.4g×
-14.4g×![]() =6.4g,故氧化物中氮氧原子个数比为
=6.4g,故氧化物中氮氧原子个数比为![]() ,故为NO2,故C错。
,故为NO2,故C错。
D、根据质量守恒,化学反应前后元素质量不变,故硝酸铵中氢元素质量等于水中氢元素质量,设硝酸铵质量为x,则x×![]() =14.4g×
=14.4g×![]() ,则x=32g,则m=32g-14.4g-9.2g=8.4g,D正确。
,则x=32g,则m=32g-14.4g-9.2g=8.4g,D正确。
故选:D。
![]()

 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案【题目】阅读下面科普短文,回答问题。
土豆是继水稻、小麦、玉米之后的第四大粮食作物,含淀粉、蛋白质、维生素C等多种营养物质,是餐桌上的美味食材。

表1鲜土豆中主要营养物质的含量(每100g)
蛋白质/g | 脂肪/g | 淀粉/g | 钙/mg | 磷/mg | 维生素C/mg |
1.5-2.3 | 0.4-0.94 | 17.5-28.0 | 11-60 | 15-68 | 20-40 |
土豆切开后发生褐变,用水浸泡能防止褐变,但会引起营养物质流失。用土豆片进行实验,测得其食用品质、淀粉含量和维生素C含量随浸泡时间的变化如下:

土豆变绿、发芽时,龙葵素含量显著增高,而龙葵素多食可导致中毒,就算是把变绿、发芽的部位削掉,也不宜食用。除食用外,土豆还可以作为原料广泛用于医药、化工、纺织、造纸等工业中。
依据文章内容回答下列问题。
(1)表1中新鲜土豆中营养物质含量最高的是_________。
(2)由图1可知:60min内,_____ (填序号,下同)。
A 浸泡30min比10min脆性分值高
B 浸泡10min,硬度、咬碎感均无明显变化
C 随着浸泡时间的增加,粘结性、弹性分值均降低
(3)由图2可知:土豆片的淀粉含量与浸泡时间的关系是___。
(4)变绿、发芽的土豆不宜食用,其原因是_________。
(5)下列说法正确的是___________。
A 土豆是四大粮食作物之一
B 土豆中维生素C含量最高
C 用水泡可防止土豆片褐变
D 士豆开发应用的前景广阔