题目内容
【题目】定量研究对于化学科学发展有重大作用因此我们应该掌握好有关质量守恒定律的相关知识。
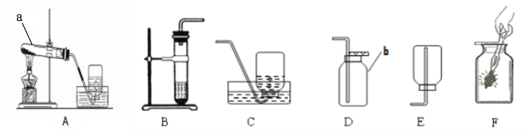
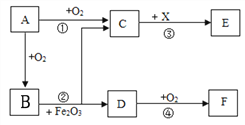
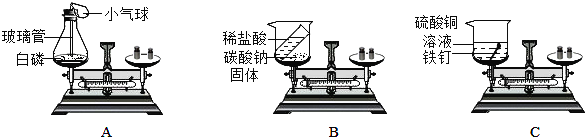
(1)如图 A、B、C 三个实验用于验证质量守恒定律(B中反应的化学方程式为: Na2CO3+2HCl=2NaCl+H2O+CO2↑,C 中反应的化学方程式为:Fe+CuSO4=FeSO4+Cu),A 中小气球的作用 为______,有关反应的化学方程式为______。三个实验中不能达到实验目的是______(选填序),理由是______。
(2)根据质量守恒定律判断,化学反应前后肯定没有变化的是______(填序号)。
①原子数目②分子数目③元素种类④物质种类⑤原子种类⑥物质的总质量
(3)自然界中绿色植物的光合作用可用下式表示:CO2+H2O ![]() 淀粉+O2,淀粉中一定含有的元素是______(填元素符号),可能含有的元素是______(填元素符号)。
淀粉+O2,淀粉中一定含有的元素是______(填元素符号),可能含有的元素是______(填元素符号)。
(4)在一个密闭容器内有 X、Y、Z、Q 四种物质,在一定条件下充分反应,测得反应前后各物质的 质量如表:试推断该容器内发生反应的基本类型为________

【答案】缓冲作用 4P+5O2![]() 2P2O5 B 反应生成的二氧化碳逸出装置外 ①③⑤⑥ C、 H O 分解反应
2P2O5 B 反应生成的二氧化碳逸出装置外 ①③⑤⑥ C、 H O 分解反应
【解析】
(1)白磷燃烧,放出热量,锥形瓶内的气压增大,所以A中小气球的作用为缓冲作用,白磷和氧气在点燃的条件下生成五氧化二磷,化学方程式为:4P+5O2![]() 2P2O5;用图A中的装置进行验证质量守恒定律,能达到目的,原因在于装置是密封的;图B不能达到目的,因为生成的二氧化碳气体散逸到空气中去了;图C也能达到目的,因为生成物和反应物中都没有气体产生,能将反应物和生成物质量全部计算在内。所以不能达到实验目的是:B,理由是:反应生成的二氧化碳逸出装置外;
2P2O5;用图A中的装置进行验证质量守恒定律,能达到目的,原因在于装置是密封的;图B不能达到目的,因为生成的二氧化碳气体散逸到空气中去了;图C也能达到目的,因为生成物和反应物中都没有气体产生,能将反应物和生成物质量全部计算在内。所以不能达到实验目的是:B,理由是:反应生成的二氧化碳逸出装置外;
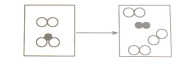
(2)化学变化后生成了新物质,物质的种类一定会发生改变;化学反应的实质是分子分成原子,原子再重新组合成新的分子,所以反应前后分子的种类一定会发生改变;化学反应前后物质的总质量不变,原子的种类、数目、元素的种类都不会发生改变;分子个数可能发生改变;所以在化学变化前后①③⑤⑥一定不变;
(3)由于二氧化碳和水中含有碳、氢、氧三种元素,根据质量守恒定律,反应前后元素的种类不变,生成物中也一定含有碳、氢、氧元素,氧气中含有氧元素,因此淀粉中一定含有碳、氢元素,可能含有氧元素;
(4)根据质量守恒定律可知,反应后X的质量=反应前X、Y、Z、Q四种物质的质量总和-反应后Y、Z、Q三种物质的质量总和,即反应后X物质的质量为=(2+2+84+5)g-(24+0+14)g=55g,反应后Z质量减少是反应物,X、Y、Q质量增加是生成物,该反应是一种物质生三种物质,属于分解反应。