题目内容
【题目】某溶液M可能含有盐酸、硫酸、氯化钠、硝酸镁中的一种或几种,为了探究其组成,向一定质量的溶液M中逐滴加入氢氧化钡溶液,生成沉淀的质量与所加氢氧化钡溶液的质量之间的关系如图所示。下列相关说法不正确的是
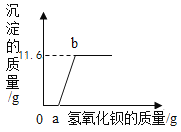
A.从图象分析,加入一定质量的氢氧化钡后开始生成沉淀,11.6g沉淀全部是氢氧化镁
B.溶液M中一定不含有硫酸,可能含有氯化钠
C.到达b点时所得溶液中的阴离子可能含有氯离子和硝酸根离子
D.到达b点时所消耗氢氧化钡溶液中溶质的质量大于34.2g
【答案】C
【解析】
硫酸根离子和钡离子一接触就会生成硫酸钡沉淀,镁离子和氢氧根离子反应会生成氢氧化镁沉淀,氢离子和氢氧根离子反应生成水,加入一定量的氢氧化钡才会生成沉淀,说明M中一定不含硫酸,一定含有盐酸、硝酸镁,可能含有氯化钠。加入氢氧化钡溶液后,氢氧化钡先与盐酸反应,等盐酸完全消耗后,氢氧化钡与硝酸镁反应生成氢氧化镁沉淀和氯化钡。
根据以上分析可知:
A、从图像分析,加入一定质量的氢氧化钡后开始生成沉淀,11.6g沉淀全部是氢氧化镁,故A正确;
B、溶液M中一定不含有硫酸,可能含有氯化钠,故B正确;
C、盐酸和氢氧化钡反应生成氯化钡和水,氢氧化钡和硝酸镁反应生成氢氧化镁沉淀和硝酸钡,所以到达b点时所得溶液中的阴离子一定含有氯离子和硝酸根离子,故C错误;
D、与硝酸镁反应的氢氧化钡的质量为x
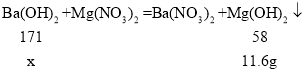
![]() x=34.2g
x=34.2g
氢氧化钡既要与稀盐酸反应,也要与硝酸镁反应,所以到达b点时所消耗氢氧化钡溶液中溶质的质量大于34.2g,故D正确。故选C。

 智慧小复习系列答案
智慧小复习系列答案【题目】在化学实验课上,小组同学利用回收的二氧化锰来催化过氧化型制取氧气,但发现利用回收的二氧化锰作为催化剂反应速率很慢.查阅资料得知:催化剂在催化过程中催化剂的活性减弱或失去,这种现象叫做催化剂的中毒.为了探究影响二氧化锰催化能力降低的因素,在老师的指导下,小组同学进行如下实验:
(实验准备)
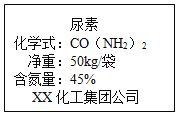
取三份质量均为1克的二氧化锰分别催化50毫升溶质质量分数为5%、15%、25%的过氧化氢溶液分解,试验后回收二氧化锰,并分别标为②、③、④;另取多次催化分解5%过氧化氢实验后回收的二氧化锰,标为⑤。
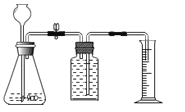
(实验步骤)
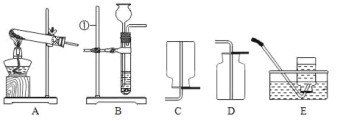
(1)连接仪器,检查装置气密性,检查该实验气体发生装置气密性的方法是_______。
(2)取未使用过的二氧化锰0.5克,标为①,加入锥形瓶中,再加入10毫升溶质质量分数为5%的过氧化氢溶液,记录收集20s时间气体的体积.
(3)再分别取②、③、④、⑤组二氧化锰各0.5克,重复上述实验。
(4)采取多次实验取平均值的方法,实验数据记录如下:
组别 | ① | ② | ③ | ④ | ⑤ |
收集气体体积/ml | 118 | 92 | 87 | 77 | 62 |
(回答下列问题)
①实验过程中量筒的作用是________
②实验中,除了通过比较收集相同时间内产生的气体体积,还可以通过比较_________来对比二氧化锰的催化效果。锥形瓶中残留的空气对测量结果_________(填“有”或“没有”)。
③请写出该实验反应的符号表达式__________
(5)由表中实验_______(填实验序号)数据可知,影响回收的二氧化锰催化效率下降的因素有二氧化锰的使用次数。由表中实验数据②、③、④数据可知,影响回收的二氧化锰催化效率下降的因素是______
(进一步探究)化学课本告诉我们,硫酸铜溶液也可以催化过氧化氢溶液的分解。小明通过前面的学习想知道硫酸铜是离子构成的,想知道硫酸铜溶液中的哪种粒子对过氧化氢溶液分解有催化作用产生了好奇。
(查阅资料)硫酸铜溶液中有铜离子、硫酸根离子和水分子;硫酸钠溶液中有钠离子,硫酸根离子和水分子。
(实验设计)
①根据所学知识判断水分子对过氧化氢分解_______(填“有”或“没有”)催化作用。
②提供药品:5%的过氧化氢溶液、硫酸铜溶液、硫酸钠溶液,仪器自选。请设计实验欲证明是铜离子对过氧化氢有催化作用____________(包括操作、现象、结论)。