��Ŀ����
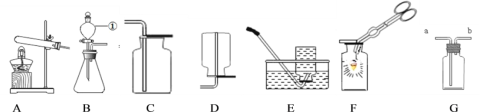
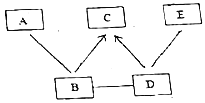
����Ŀ����ͼ��A-E�dz��л�ѧ���������ֲ�ͬ��������,E�Ǵ���Ȼ������ȡ����ߵĽ�����ͼ�С�----����ʾ����������֮���������Һ�з�����ѧ��Ӧ,��������ʾ��ij�����ʿ�ͨ��һ����Ӧֱ��ת��Ϊ��һ������(���ַ�Ӧ������P��Ӧ��������ȥ)������д���пո�
��1��C���ʿ�����________(��дһ�����ʵĻ�ѧʽ),D���ʿ�����________(��дһ�����ʵĻ�ѧʽ).
��2��д��һ��D��E��Ӧ�Ļ�ѧ����ʽ_____________________.
��3��д��һ��A��B��Ӧ�Ļ�ѧ����ʽ_____________________.
���𰸡�H2O���������ɣ� HCl���������ɣ� Fe+2HCl��FeCl2+H2�����������ɣ� 2NaOH+CuSO4��Cu��OH��2��+Na2SO4���������ɣ�
��������
A��E�dz��л�ѧ���������ֲ�ͬ�������ʣ�E�Ǵ���Ȼ������ȡ����ߵĽ���������E������D��������Ӧ������D���������ᣬB����D��Ӧ�����������������Ʒ�Ӧ��B�������������ƣ�B��D����ת��ΪC���������ơ����ᶼ����ת����C������C������ˮ��A����Ӧ������A����������ͭ��������֤���Ƶ���ȷ��
�������Ϸ�����֪��
��1��C���ʿ�����H2O��D���ʿ�����HCl��
��2��D��E�ķ�Ӧ�������������ᷴӦ�����Ȼ���������������ѧ����ʽΪ��Fe+2HCl��FeCl2+H2����
��3��A��B�ķ�Ӧ���������ƺ�����ͭ��Ӧ���������ƺ�������ͭ����ѧ����ʽΪ��2NaOH+CuSO4��Cu��OH��2��+Na2SO4��

 ��1����Ԫ�¿�������ĩϵ�д�
��1����Ԫ�¿�������ĩϵ�д�����Ŀ���ִ�������,����Խ��Խע����Ԫ�ص���ȡ����Ԫ�ض����彡����������Ҫ�����á��±���ij���г����۵�һ�����ӵ�ʳ������װ���ϵIJ���˵����
���� | �Ȼ��ơ������KIO3 |
������ | 20mg-30mg/kg |
������ | 18���� |
ʳ�÷��� | ��ʱ������ |
���淽�� | �ܹ⡢���ȡ��ܷ⡢���� |
��ش��������⣺�����ڣ�1��С����,���������д��������̣�
��1����ʳ�÷��������淽�����Ʋ����صĻ�ѧ����֮һ��______��
��2����������KIO3��,��Ԫ�ء���Ԫ�ء���Ԫ�ص�������______��
��3����������KIO3��,��Ԫ�ص���������______����ȷ��0.01%
��4������1kg������ʳ����,Ӧ����______g�����,����ߺ��������㣻��ȷ��0.01%
��5���������������������,��Ҫ����0.15mg�ĵ�Ԫ��,��Ӧ����üӵ�ʳ��______g��
����Ŀ��ѧϰ��MnO2�Թ�������ֽ��д����õ�֪ʶ��ijͬѧ�룺CuO�ܷ�������MnO2�Ĵ��������أ����ǽ���������̽����
�����룩��CuO���Ǵ�����Ҳ�����뷴Ӧ����Ӧǰ�������ͻ�ѧ���ʲ��䣻
��CuO���뷴Ӧ����O2����Ӧǰ�������ͻ�ѧ���ʷ����˸ı䣻
��CuO�Ƿ�Ӧ�Ĵ�������Ӧǰ��__________________��
��ʵ�飩����ƽ����0.2gCuO��ȡ5mL5%�Ĺ���������Һ���Թ��У���������ʵ�飺

��1��������
��������� | ������ | ��������� | ���� |
____________�����ǵ�ľ����ȼ�� | ________ | ��Һ�������ݷų��� ___________ | ������������������������������ |
��2������ٵ�Ŀ����_____________________��
��3�����������ܱ�CuO���ֽ�ų�O2�����ֱ���ʽΪ________________������CuO�Է�Ӧ���ɵ������Ķ���________��������������������Ӱ�졣