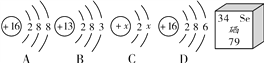题目内容
【题目】大卫同学欲配制一定溶质质量分数的NaCl溶液,他准备了下列实验仪器。
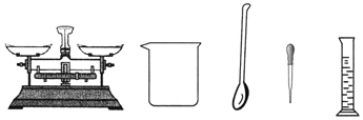
请填空:
(1)配制时可按下列实验步骤进行:计算→称量→ 量取 →____________;
(2)称量时,__________________应放在托盘天平左盘的纸片上;
(3)配制过程中为促进NaCl的溶解,还需要的一种玻璃仪器是___________(填仪器名称);
(4)量取一定体积的水,量液时,量筒必须放平,视线要与量筒内液体的凹液面的___________保持水平。
【答案】溶解 NaCl固体粉末 玻璃棒 最低处
【解析】
(1)配制一定溶质质量分数的NaCl溶液,首先计算配制溶液所需NaCl和水的质量,再称量所需的NaCl和量取水,最后进行溶解;
(2)托盘天平的使用要遵循“左物右码”的原则,称量氯化钠时应放在托盘天平左盘的纸片上;
(3)配制过程中为促进NaCl的溶解,还需要的一种玻璃仪器是玻璃棒,作用是搅拌,加快溶解速率;
(4)量取一定体积的水,量液时,量筒必须放平,视线要与量筒内液体的凹液面的最低处保持水平。

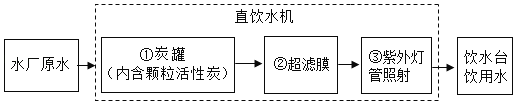
【题目】化学用语是学习化学的基本工具。请用化学符号或化学式填空:
(1)氯化钠______(2)标出过氧化氢中氧元素的化合价_________
(3)氩气_______(4)2个钾离子__________
【题目】现有H2SO4和CuSO4的混合溶液,为了测定CuSO4的质量分数,小明同学进行如下实验:
取混合溶液于烧杯中,向其中加入铁片至完全反应。反应前后,有关数据如表。
烧杯 | 原混合溶液 | 加入的铁片 | 反应后烧和烧杯内物质的总质量(克) | 剩余铁片 | 析出铜 | |
质量(克) | 80 | 100 | 20 | 199.8 | 3.2 | 12.8 |
(1)实验中产生氢气的质量为______克。
(2)请根据实验数据计算原混合溶液中CuSO4的质量分数______。
(3)小红同学用加入足量BaCl2溶液,通过生成BaSO4沉淀的质量来计算原混合溶液中CuSO4的质量分数,请分析是否合理并说明原因______。