题目内容
【题目】下列实验现象描述正确的是
A.硫燃烧后生成有刺激性气味的气体 B.木炭燃烧后生成黑色固体
C.铁丝在空气中剧烈燃烧,火星四射 D.红磷在空气中燃烧产生白雾
【答案】A
【解析】
试题分析:B中木炭燃烧生成一种能使澄清石灰水变浑浊的气体,B错误;铁丝在氧气中剧烈燃烧,C错误;红磷燃烧产生大量的白烟,D错误。故选A。

 名校课堂系列答案
名校课堂系列答案【题目】碳酸氢钠是小苏打的主要成分,在生产和生活中有许多重要的用途。化学课上,同学们为了解碳酸氢钠的性质,将一定质量的碳酸氢钠和稀硫酸混合,充分反应后,有气体逸出,写出该反应的化学方程式_______,同学们对反应后溶液中溶质的成分进行了探究:认为除一定含有硫酸钠外可能还含有其他成分,因此进行了猜想并做了如下实验:
【实验用品】pH试纸、锌片、氧化铜粉末、稀硫酸、氢氧化钠溶液、氯化钡溶液。
【猜想与假设】反应后溶液中溶质的可能组成成分
猜想一:硫酸钠 猜想二:硫酸钠、碳酸氢钠 猜想三:硫酸钠、硫酸
【实验探究】同学们取反应后的溶液用不同方案进行如下实验,请根据结论完成下表实验现象中的①②③。
实验方案 | A | B | C | D | |
实验操作 |
|
|
|
| |
实验现象 | ① | 产生白色沉淀 | 试纸变色,对照标准比色卡,pH ②7 | ③ | |
实验结论 | 猜想二不正确 | 猜想三正确 | 猜想三正确 | 猜想三正确 | |
【得出结论】猜想三正确。
【评价反思】
(1)老师对同学们能用多种方案进行探究,并且得出正确的实验结论给予了肯定,同时指出探究中存在一处明显操作错误是:__________;
(2)有同学对实验方案B的结论提出了质疑,认为仅凭此现象不能得出猜想三正确,请说明理由________。
【总结提高】依据所给实验用品,设计不同的方案确认猜想三是正确的。请写出你的实验方案________。
【题目】某工业铁红(Fe2O3)样品中可能混有一种黑色的金属氧化物杂质。根据工业制取铁红的流程分析,该杂质可能是FeO或CuO。兴趣小组同学为探究样品中是否含有杂质及杂质的成分,进行如下实验。
(1)甲组同学分别取质量相等的样品和Fe2O3,加入试管Ⅰ、Ⅱ中,然后加入等体积稀硫酸进行如图对照实验,并得出结论:样品中不含杂质。你认为该结论_______(填“合理”或“不合理”)。
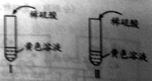
(2)乙组同学按下列步骤进行实验:
【收集资料】
①上述三种氧化物在加热条件下,都能与氢气反应得到相应的金属单质和水。
②三种氧化物中氧元素的质量分数由大到小的顺序为____________。
③铁粉中混有少量铜时,难以从金属颜色确定是否含有金属铜。
【设计方案进行实验】
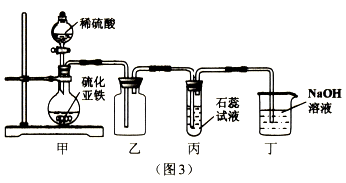
乙组同学用下图装置进行实验(碱石灰是氧化钙与氢氧化钠固体混合物)。
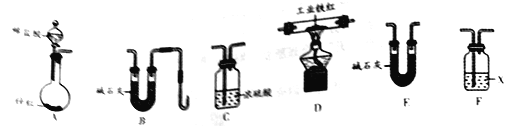
①乙组同学的实验装置中,依次连接的合理顺序为A→F→_____→_______→______→B。检验装置气密性后,向各装置中加入药品。装置F中试剂X是_____溶液,装置C的作用是___________。
②下列实验操作步骤的合理顺序是________(填写操作编号)。
a.加热装置D中反应管 b.检验H2的纯度
c.打开装置A中分液漏斗的活塞,向圆底烧瓶中加入稀盐酸
③该实验处理问起的方法是______________。
【实验分析与结论】
乙组同学的两次实验数据如下表:(两次实验工业铁红均与氢气完全反应)
实验编号 | 加入装置D中工业铁红的质量(g) | 实验后装置E的增重(g) |
1 | 8.0 | 2.6 |
2 | 16.0 | 5.2 |
①分析数据,你的实验结论是_________________。
②请帮助乙组同学设计实验方案确认该样品中杂质的成分________________。(写出操作、现象和结论,若该样品中不含杂质本题不必作答)