题目内容
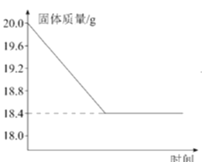
【题目】小明同学加热实验室某不纯的KMnO4固体分解制备O2(杂质可溶于水且受热不分解),完全反应后测得相关数据如图所示。回答下列问题:
(1)将分解后剩余固体加水充分溶解,经过滤、洗涤、干燥得到的固体为______(填化学式),在另两种实验室制备O2的方法中,该物质被用作__________。
(2)该分解过程生成的O2的质量为________g。
(3)计算该固体中KMnO4的质量分数(写出计算过程)。
【答案】MnO2;催化剂;1.6g;79%(详见解析)
【解析】
(1)由题意可知,该图像是高锰酸钾制取氧气,化学方程式为:2KMnO4![]() K2MnO4+MnO2+O2↑,由图像可知高锰酸钾全部分解,完全反应后加入水充分溶解,题干中说明杂质可以溶于水,生成物中只有二氧化锰不溶于水,二氧化锰在过氧化氢和氯酸钾制取氧气中起到了催化作用。将分解后剩余固体加水充分溶解,经过滤、洗涤、干燥得到的固体为MnO2,在另两种实验室制备O2的方法中,该物质被用作催化剂;
K2MnO4+MnO2+O2↑,由图像可知高锰酸钾全部分解,完全反应后加入水充分溶解,题干中说明杂质可以溶于水,生成物中只有二氧化锰不溶于水,二氧化锰在过氧化氢和氯酸钾制取氧气中起到了催化作用。将分解后剩余固体加水充分溶解,经过滤、洗涤、干燥得到的固体为MnO2,在另两种实验室制备O2的方法中,该物质被用作催化剂;
(2)由图像可知,反应前后固体质量共减少了20-18.4=1.6g,该反应中只生成了氧气,没有生成其他气体或者液体,所以生成的氧气的质量为1.6g;
(3)由题意可知,生成的氧气是由高锰酸钾分解得到。
设高锰酸钾的质量为x。
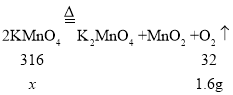
![]()
x=15.8g;
原固体样品中高锰酸钾的质量为15.8g,由图象可知原固体样品为20g,所以该固体中KMnO4的质量分数为![]() ×100%=79%;
×100%=79%;
答:该固体中KMnO4的质量分数为79%。

练习册系列答案
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案
相关题目