题目内容
【题目】同学们为了证明CO2与NaOH溶液能否反应进行了如下探究:
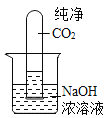
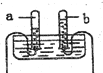
活动一:依据装置中气体体积或压力的变化判断是否反应。
资料:通常情况下,1体积水可以溶解1体积CO2。
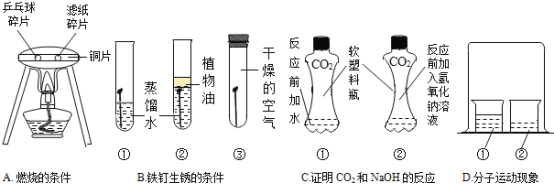
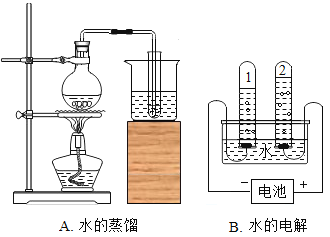
甲同学要用如图所示装置证明CO2与NaOH溶液能够反应,可以观察到的现象是_____。
乙同学认为甲同学的实验不足以证明CO2与NaOH溶液能够反应,应该再把NaOH溶液换为水做对比实验。
请通过甲乙两位同学实验的对比,我们能否证明CO2能与NaOH溶液反应?说出你的理由_____。
活动二:从生成物角度判断是否反应。
同学们提出:以甲实验试管所得液体为研究对象。通过检验样品中是否含有Na2CO3来证明CO2能否与NaOH溶液反应。
资料:Ca(OH)2是微溶物,Ca2+和OH—不能大量共存于溶液中。
丙、丁两位同学分别进行了如下实验:
操作 | 现象 | |
丙 | 取2―3mL样品,向其中逐滴加入稀盐酸 | 开始偶有少量气泡后来有大量气泡 |
丁 | 取2―3mL稀盐酸,向其中逐滴加入样品 | 开始即有大量气泡 |
请
(1)为什么丙、丁两位同学的实验现象不同_____?
(2)丙同学的实验里不能用酚酞试液替代稀盐酸,理由是_____。
(3)还有什么物质(酸类物质除外)可以代替丙实验的盐酸来检验样品中是否含有Na2CO3?请列举一例:_____。
活动三:实验拓展
已知:碳酸钠稳定,受热难分解。有同学提出取少量甲、乙实验试管里的液体进行如下图所示实验也能判断CO2能否与NaOH溶液反应。可以观察到:甲试管内壁仅出现少量气泡;乙试管内壁出现较多气泡。
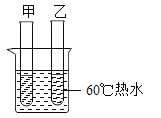
(1)这种加热方式叫热水浴,与直接用酒精灯加热相比,热水浴的优点有哪些?_____、_____(答两点)。
(2)该实验为什么能证明CO2与NaOH溶液发生了反应_____?
【答案】试管内液体会上升至试管顶部(液体充满试管) 能证明,因为甲乙实验里试管中液面上升的高度不同(或甲实验试管里液面上升的速度比乙快);或不能证明,因为CO2也可能是溶解在NaOH溶液中了,使得甲乙液面同样上升 丙开始阶段氢氧化钠和碳酸钠多,盐酸少,丁开始阶段盐酸多,少氢氧化钠和碳酸钠(此处不要求学生知道氢氧化钠与碳酸钠谁优先与盐酸反应,也不要求学生知道碳酸钠与盐酸反应是否经历由碳酸钠到碳酸氢钠的过程) 样品中可能有NaOH,可使试液显红色(NaOH可以干扰碳酸钠的检验) BaCl2溶液、Ba(NO3)2溶液任一即可(“溶液”二字不做为给分点) 受热均匀 便于控制温度 甲试管原有的CO2与NaOH溶液反应生成碳酸钠,碳酸钠稳定不分解。热水浴后甲试管内壁的少量气泡是原氢氧化钠溶液中溶解的空气受热后逸出造成的(该问题学生答出上面两句话中的任何一句即可得满分)。乙试管较多的气泡是溶于水的CO2气体受热后溶解度变小逸出造成的(学生答H2CO3不稳定易分解放出CO2气体也给分)。
【解析】
活动一:二氧化碳和氢氧化钠反应生成的碳酸钠,试管内液面上升,烧杯内液面下降;
通过甲乙同学对比,能证明CO2与NaOH溶液能够反应,因为甲乙实验里试管中液面上升的高度不同(或甲实验试管里液面上升的速度比乙快);或不能证明,因为CO2也可能是溶解在NaOH溶液中了,使得甲乙液面同样上升;
活动二:(1)丙丁同学的实验现象不同的原因是因为稀盐酸加入顺序和量不同,丙同学加入稀盐酸,开始阶段氢氧化钠和碳酸钠多,盐酸少,稀盐酸先和氢氧化钠反应再和碳酸钠反应,而丁同学正好一次性的加入稀盐酸量多,少氢氧化钠和碳酸钠,反应迅速;
(2)碳酸钠溶液也显碱性,样品中可能有NaOH,可使试液显红色;
(3)BaCl2溶液、Ba(NO3)2都能和碳酸钠反应生成生成白色沉淀;
活动三:(1)热水浴的优点:受热均匀、安全;
(2)甲试管原有的CO2与NaOH溶液反应生成碳酸钠,碳酸钠稳定不分解。热水浴后甲试管内壁的少量气泡是原氢氧化钠溶液中溶解的空气受热后逸出造成的;乙试管较多的气泡是溶于水的CO2气体受热后溶解度变小逸出造成的;故该实验能证明CO2与NaOH溶液发生了反应。

 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案