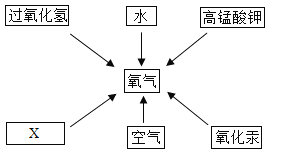
题目内容
【题目】向某硫酸和硫酸铜的混合溶液中加入某浓度的氢氧化钠溶液,产生沉淀的质量与加入氢氧化钠溶液的质量关系如图所示。下列说法正确的是( )
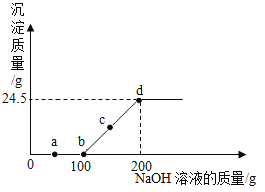
A.a点溶液中含有两种溶质
B.c点溶液中主要存在的离子为Na+ 、Cu2+、OH-、SO42-
C.bc段发生反应的类型为置换反应
D.根据图中数据可以计算出氢氧化钠溶液的浓度
【答案】D
【解析】
氢氧化钠加入硫酸和硫酸铜的混合溶液中,先与硫酸反应产生硫酸钠和水,后与硫酸铜反应产生硫酸钠和氢氧化铜沉淀;
A、a点时溶液中的硫酸未反应完全,溶液中含有硫酸、硫酸铜以及硫酸和氢氧化钠反应生成的硫酸钠,共三种溶质;故选项错误;
B、c点时,硫酸反应完全,硫酸铜部分反应,溶液中主要存在的离子为Na+ 、Cu2+、SO42-
C、bc段氢氧化钠与硫酸铜反应产生硫酸钠和氢氧化铜沉淀,2NaOH+CuSO4=Na2SO4+Cu(OH)2↓该反应属于复分解反应;故选项错误;
D、根据图中产生氢氧化铜沉淀24.5g,
解:设与硫酸铜反应的氢氧化钠溶液溶质质量为x。
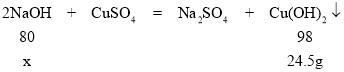
![]() x=20g
x=20g
氢氧化钠溶液的浓度=![]() 。
。
故选项正确;
故选:D。

 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案【题目】同学们为了证明CO2与NaOH溶液能否反应进行了如下探究:
活动一:依据装置中气体体积或压力的变化判断是否反应。
资料:通常情况下,1体积水可以溶解1体积CO2。
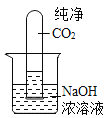
甲同学要用如图所示装置证明CO2与NaOH溶液能够反应,可以观察到的现象是_____。
乙同学认为甲同学的实验不足以证明CO2与NaOH溶液能够反应,应该再把NaOH溶液换为水做对比实验。
请通过甲乙两位同学实验的对比,我们能否证明CO2能与NaOH溶液反应?说出你的理由_____。
活动二:从生成物角度判断是否反应。
同学们提出:以甲实验试管所得液体为研究对象。通过检验样品中是否含有Na2CO3来证明CO2能否与NaOH溶液反应。
资料:Ca(OH)2是微溶物,Ca2+和OH—不能大量共存于溶液中。
丙、丁两位同学分别进行了如下实验:
操作 | 现象 | |
丙 | 取2―3mL样品,向其中逐滴加入稀盐酸 | 开始偶有少量气泡后来有大量气泡 |
丁 | 取2―3mL稀盐酸,向其中逐滴加入样品 | 开始即有大量气泡 |
请
(1)为什么丙、丁两位同学的实验现象不同_____?
(2)丙同学的实验里不能用酚酞试液替代稀盐酸,理由是_____。
(3)还有什么物质(酸类物质除外)可以代替丙实验的盐酸来检验样品中是否含有Na2CO3?请列举一例:_____。
活动三:实验拓展
已知:碳酸钠稳定,受热难分解。有同学提出取少量甲、乙实验试管里的液体进行如下图所示实验也能判断CO2能否与NaOH溶液反应。可以观察到:甲试管内壁仅出现少量气泡;乙试管内壁出现较多气泡。
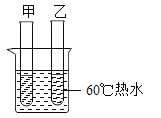
(1)这种加热方式叫热水浴,与直接用酒精灯加热相比,热水浴的优点有哪些?_____、_____(答两点)。
(2)该实验为什么能证明CO2与NaOH溶液发生了反应_____?
【题目】“低钠盐”可以控制钠的摄入量从而防治高血压等疾病。制备“低钠盐”是在食盐中用NaCl按照配方比例添加食用KCl。国内某些生产厂家为改变“低钠盐”口味还会加入少量镁盐(仅限MgSO4或MgCl2)。
(1)测得某“低钠盐”样品a中只含有NaCl和KCl,该样品中的NaCl和KCl溶于
水时解离出的阴离子都是___________(填离子符号)。
(2)探究某“低钠盐”样品b中是否添加有镁盐,以及添加的是何种镁盐?
【猜想】I、不含镁盐 Ⅱ、含有硫酸镁 Ⅲ、含有氯化镁

【进行实验】
(3)请完成下表(已知BaSO4是难溶于水和酸的白色固体):
假设和现象 | 判断和化学方程式 | |
① | 若现象a为白色沉淀 | 则猜想____不成立。 |
② | 若现象a为_________, 现象b为_________。 | 则猜想Ⅲ成立。写出无色溶液B与硝酸中和反 应的化学方程式_________________。 |
③ | 若现象a、b均 为:产生白色沉淀 | 则猜想____成立。写出无色溶液B与硝酸钡溶液 反应的化学方程式______________。 |