题目内容
【题目】烧碱、熟石灰是两种重要的碱,回答与它们有关的下列问题。
(1)用于改良酸性土壤是熟石灰、烧碱中的_______;
(2)实验室常用石灰水来检验二氧化碳气体,其发生反应的化学方程式是_______;
(3)烧碱溶液、石灰水都能使无色酚酞溶液变红、与酸反应生成盐和水、与某些盐反应生成新盐和新碱,从微观角度看它们具有这些相似化学性质的原因是_______;
【答案】熟石灰 ![]() 溶液中都含有氢氧根离子
溶液中都含有氢氧根离子
【解析】
(1)改良酸性土壤用熟石灰,不用烧碱,烧碱碱性太强,故填:熟石灰。
(2)实验室常用石灰水来检验二氧化碳气体,二氧化碳能使澄清石灰水变浑浊,石灰水的主要成分是氢氧化钙,二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,反应的化学方程式:![]() 。
。
(3)烧碱是氢氧化钠,石灰水的主要成分是氢氧化钙,氢氧化钠和氢氧化钙具有相似的化学性质是都含有氢氧根离子,故填:溶液中都含有氢氧根离子。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
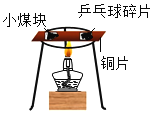
小学生10分钟应用题系列答案【题目】某化学兴趣小组同学将铜丝绕成螺旋状后,在酒精灯火焰上加热,铜丝变黑后,趁热插入疏松的氯化铵(NH4Cl)固体里,变黑的铜丝又变回紫红色。他们对此产生了兴趣,于是在老师的指导下进行如下探究:
(查阅资料)(1)氯化铵受热易分解,反应的化学方程式为:NH4Cl![]() NH3↑+HCl↑;
NH3↑+HCl↑;
(2)NH3+HCl=NH4Cl;
(3)无水硫酸铜为白色固体,遇水会变成蓝色。
(提出问题)使氧化铜还原为铜的是什么物质?
(作出猜想)猜想一:CO 猜想二:HCl 猜想三:NH3
小晶认为猜想一不合理,理由是_________。
(实验探究)兴趣小组同学按如下装置进行实验(夹持装置已省略):

实验操作 | 实验现象 | 实验结论 |
将氯化氢气体和氨气分别通入装置,点燃酒精灯加热 | 通入氯化氢气体硬质玻璃管中无明显变化,通入氨气硬质玻璃管中观察到的现象是____。 | 猜想三成立 |
(反思与评价)
(1)通入氨气,观察到乙中固体变蓝,同时生成一种化学性质不活泼的气体。则氨气还原氧化铜的化学方程式为______。氨气有强烈的刺激性气味,对人体有害,则该装置存在的不足之处是________。
(2)小明认为实验室可用加热氯化铵的方法制取氨气,你认为该方法是否合理_________(填“合理”或“不合理”)。
(拓展延伸)“焊药”中含有氯化铵(NH4Cl),“焊药”的主要作用是清除焊接处金属表面生成的金属氧化物,确保焊接牢固。
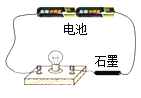
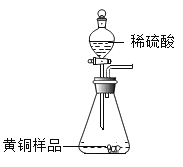
【题目】西汉东方朔所撰的《申异经》中有“西北有宫,黄铜为墙,题曰地皇之宫”的记载。黄铜是铜锌合金。为测定某黄钢样品中铜的质量分数,某同学取黄铜样品与足量稀硫酸充分反应(如图所示),测得相关数据如表。
反应前 | 反应后 | ||
装置质量 | 黄铜样品质量 | 稀硫酸质量 | 装置及装置内物质的总质量 |
260.0g | 50.0g | 100.0g | 409.5g |
计算:
(1)实验过程中,产生氢气的质量为 g。
(2)该黄铜样品中铜的质量分数(计算结果精确到0.1%)。
【题目】某兴趣小组对石灰石样品进行如下实验:取12g样品放人烧杯中,将100g稀盐酸分4次加入,充分反应后(杂质不溶于水,也不与酸反应),测得剩余固体的质量记录如下:
次数 | 1 | 2 | 3 | 4 |
加入稀盐酸的质量/g | 25 | 25 | 25 | 25 |
剩余固体的质量/g | 8 | 4 | 2 | 2 |
请计算:
(1)样品中碳酸钙的质量为
(2)第4次加入稀盐酸后所得溶波中CaCl2的质量分数。(写出计算过程,最终结果保留0. 1%)。