题目内容
【题目】某兴趣小组对石灰石样品进行如下实验:取12g样品放人烧杯中,将100g稀盐酸分4次加入,充分反应后(杂质不溶于水,也不与酸反应),测得剩余固体的质量记录如下:
次数 | 1 | 2 | 3 | 4 |
加入稀盐酸的质量/g | 25 | 25 | 25 | 25 |
剩余固体的质量/g | 8 | 4 | 2 | 2 |
请计算:
(1)样品中碳酸钙的质量为
(2)第4次加入稀盐酸后所得溶波中CaCl2的质量分数。(写出计算过程,最终结果保留0. 1%)。
【答案】(1)10(2)10.5%
【解析】
(1)根据前两次都是固体减少4g,而第三次只减少2g,说明此时已经完全无反应,说明剩余的固体为杂质,碳酸钙的质量为12g-2g=10g;
(2)设生成的氯化钙的质量为 x,生成的二氧化碳的质量为 y,
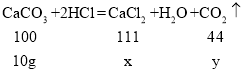
![]()
![]()
x=11.1g,y=4.4g ,
第 4 次加入稀盐酸后所得溶液中 CaCl2 的质量分数为:
![]()
答:第 4 次加入稀盐酸后所得溶液中 CaCl2质量分数为 10.5%。

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目