题目内容
【题目】根据图甲和图乙回答问题。


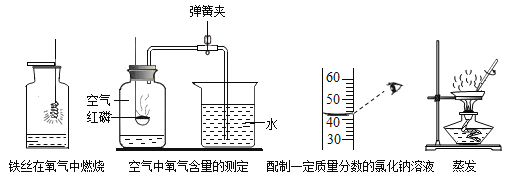
(1)图甲中A、B、C三套发生装置都可用于实验室制取气体,若制取氧气,与A装置相比,C装置的优点是_____;利用B装置制取CO2时,反应未停止前关闭止水夹,可观察到的现象是_____。
(2)为了研究二氧化碳的化学性质,某同学设计了如图乙所示的实验,D装置和F装置所装试剂_____(填“相同”或“不相同”),G装置的作用是_____;能说明与赤铁矿粉反应的气体是CO而不是CO2的实验现象是_____。
【答案】可控制反应的速率 锥形瓶中液面下降,长颈漏斗中液面升高形成液柱 相同 收集尾气,防止污染空气 D装置中的澄清石灰水没有变浑浊,装置E中的粉末由红变黑,F装置中的澄清石灰水变浑浊
【解析】
(1)C装置用分液漏斗代替长颈漏斗,可以通过分液漏斗的玻璃开关控制滴加液体药品的速率来控制反应的速率,故填可控制反应的速率;
反应未停止前关闭止水夹,锥形瓶中的二氧化碳气体在锥形瓶中滞留产生较大的压强且大于大气压,瓶内较大的压强会将锥形瓶中的液体压进长颈漏斗中,观察到的现象是锥形瓶中液面下降,长颈漏斗中液面升高形成液柱,故填锥形瓶中液面下降,长颈漏斗中液面升高形成液柱。
(2)由图可知,D装置的作用是检验二氧化碳是否除尽,其中的试剂是澄清的石灰水,F装置的作用是检验装置E中的反应是否生成二氧化碳,检验二氧化碳也是用澄清的石灰水,即D装置与F装置中的试剂相同,故填相同;
该实验后的尾气中含有残留的一氧化碳气体,直接排放会污染空气,G装置采用排水法收集尾气,可以避免尾气污染空气,所以G 的作用是收集尾气,防止污染空气,故填收集尾气,防止污染空气;
C装置中的氢氧化钠溶液吸收了原气体中的二氧化碳气体,D装置中的澄清石灰水没有变浑浊,装置E中的粉末由红变黑,说明有具还原性的气体与赤铁矿中的氧化铁发生反应,且F装置中的澄清石灰水变浑浊,说明装置E中的反应生成了二氧化碳,所以能说明与赤铁矿粉发生反应的气体是CO而不是CO2的实验现象是装置E中的粉末由红变黑,F装置中的澄清石灰水变浑浊,故填D装置中的澄清石灰水没有变浑浊,装置E中的粉末由红变黑,F装置中的澄清石灰水变浑浊。

 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案【题目】自然界并不缺少镁,缺少的是发现镁的眼睛。某化学兴趣小组开启寻镁之旅,现邀请你参与并完成相关内容。
(1)第一站:初识金属镁。(①金属镁的物理性质:____(写一条);②金属镁的化学性质:镁能与氧气反应,反应的化学方程式为___.
(2)第二站:再遇金属镁。将打磨过的镁条放入稀盐酸中,反应现象是______。化学方程式为______。
(3)第三站:制备金属镁。小组同学模拟工业上从海水晒盐剩下的苦卤中提取镁,流程如下:
![]()
流程中X为________________.
(4)第四站:再探金属镁。
(提出问题)镁能否与热水反应?如果反应,产物是什么?
(相关信息)①Mg+2H2O=Mg(OH)2+H2↑②氢氧化镁在热水中能部分溶解。
实验操作 | 实验现象 | 实验结论 |
______ | _____ | 镁能与热水反应,生成氢氧化镁和氢气 |
(5)上述寻镁之旅中你收获到镁的化学性质有_______.
【题目】小云同学完成如图实验:向盛满CO2气体的塑料瓶中加入澄清的石灰水,拧紧瓶盖振荡。让她吃惊的是瓶子虽然变瘪了,但是并没有看到白色沉淀。

(发现问题)沉淀哪去了?
(探究环节一)
提出猜想:二氧化碳没有和氢氧化钙反应,而是直接溶于水了。于是设计如下实验进行验证。
步骤 | 操作 | 实验现象 |
1 | (1)取2个相同规格的软塑料瓶, 分别集满二氧化碳气体 (2)分别向 2 个塑料瓶中注入等体积的氢氧化钙溶液和蒸馏水, 拧紧瓶盖,振荡 | 2 个塑料瓶都变瘪了,但是注入氢氧化钙溶液的塑料瓶瘪的程度更大 |
2 | (1)用pH试纸测反应前氢氧化钙溶液的酸碱度 (2)向软塑料瓶中注入适量氢氧化钙溶液震荡后,测反应后溶液的 pH 值 | 反应前氢 氧 化 钙 溶 液 的 pH 大于 7; 反应后 溶液的pH小于7 |
(1)小云预期会看到白色沉淀的依据是______________________(写出反应的化学方程式)
(2)反应后溶液的pH小于7是由于生成了____(写化学式);通过分析以上实验现象,小云得到的结论是_______________________。
(探究环节二)
查阅资料后得知:适量的二氧化碳和氢氧化钙能发生反应生成难溶于水的碳酸钙,如果二氧化碳过量,则碳酸钙会继续和二氧化碳反应生成可溶性的碳酸氢钙。(“→”代表反应的方向)CO2+CaCO3+H2O ![]() Ca(HCO3)2
Ca(HCO3)2
提出猜想:实验中可能二氧化碳过量,反应生成了碳酸氢钙,所以没有看到沉淀
步骤 | 操作 | 实验现象 |
1 | 取少量的氢氧化钙溶液于试管中,向其中持续通入CO2气体 | 开始产生白色沉淀过一会儿,白色沉淀消失 |
2 | (1)取一个软塑料瓶,集满二氧化碳气体,向其中注入少量的氢氧化钙溶液,拧紧瓶盖,振荡 (2)此时将软塑料瓶放在热水浴中加热 (3)将加热后的软塑料瓶冷却 | 瓶子变瘪 溶液变浑浊 溶液又变澄清 |
3 | (1)取一个软塑料瓶,集满二氧化碳气体,向其中注入少量的氢氧化钙溶液,拧紧瓶盖,振荡 (2)向实验后的软塑料瓶中继续滴加氢氧化钙溶液 | ? |
实验结论:猜想成立
(1)实验步骤2中“改变瓶子的温度”目的是___________。
(2)实验步骤3中看到的实验现象是________________。
【题目】常温下,往盛放适量M物质的烧杯中逐渐加入N物质并充分搅拌。右下图横坐标x表示N物质的质量,纵坐标y表示烧杯中的某物理量(见下表)。下列实验与图像对应关系合理的是

M | N | y | |
A | 水 | 氧化钙 | 溶液的温度 |
B | 水 | 氢氧化钠 | 溶液的pH |
C | 饱和氯化钠溶液 | 氯化钠 | 溶液的溶质质量分数 |
D | 硫酸铜溶液 | 铁粉 | 溶液的质量 |
【题目】(1)小明用传感器探究稀氢氧化钠溶液与稀盐酸反应过程中温度和 pH 的变化。测定结果如图所示。根据图示回答下列问题:

氢氧化钠和盐酸的反应属于______填“吸热”或“放 热”)反应。写出 61s 时,溶液中溶质的化学式_____。
(2)某化学小组用一定量的 AgNO3 和 Cu(NO3)2 的混合溶液进行了如图所示的实验,并对溶液 A 和固体 B 的成分进行了分析和实验探究。

(提出问题)溶液A中的溶质成分可能有哪些?
(做出猜想)猜想①:只有 Zn(NO3)2;
猜想②:有 Zn(NO3)2、Cu(NO3)2;
猜想③: 有 Zn(NO3)2、AgNO3;
猜想④:有 Zn(NO3)2、Cu(NO3)2、AgNO3
(交流讨论)不合理的猜想是_____(填序号),其理由是_____。
(实验探究)若猜想①成立,通过以下实验可确定固体的成分,请将下表填写完整
实验步骤 | 现象 | 有关反应的化学方程式 |
取少量固体,滴加_____ | 有气泡产生 | _____ |
(深入思考)若猜想④成立,固体 B 的成分是_____。
(3)除去 NaCl 溶液中 CaCl2 、MgCl2、Na2SO4 杂质的操作:①加过量的 NaOH 溶液;②加过量的 BaCl2 溶液;③过滤;④加适量的盐酸;⑤加过量的 Na2CO3 溶液。
(提示:Mg(NO3)2、BaSO4、BaCO3 难溶于水)写出以上操作的合理顺序_____(数字序号不能重复使用)。请写出溶液 BaCl2 与 Na2SO4 溶液反应的化学方程式_____。
(4)上述试剂中的 Na2CO3 溶液不能用 K2CO3 溶液代替,请说明原因_____。