题目内容
【题目】将一定质量的乙醇(C2H6O)和氧气置于一个封闭的容器中引燃,测得反应前后各物质的质量如下表。下列判断正确的是 ( )
物质 | 乙醇 | 氧气 | 水 | 二氧化碳 | X |
反应前质量/g | 23 | 40 | 0 | 0 | 0 |
反应后质量/g | 0 | 0 | 27 | 22 | a |
A.表中a的值为15
B.物质X是该反应的催化剂
C.物质X中可能含有氢元素
D.若起始时增加8g氧气,则无X生成
【答案】D
【解析】
A、根据质量守恒定律,则表中a的值为![]() ,不符合题意;
,不符合题意;
B、物质X反应前质量为0g,反应后质量为14g,属于生成物,不是该反应的催化剂,不符合题意;
C、乙醇中氢元素的质量为![]() ,生成物水中氢元素的质量为
,生成物水中氢元素的质量为![]() ,则物质X中不可能含有氢元素,不符合题意;
,则物质X中不可能含有氢元素,不符合题意;
D、乙醇中碳元素的质量为![]() ,含氧元素的质量为
,含氧元素的质量为![]() ;生成物水中含氧元素的质量为
;生成物水中含氧元素的质量为![]() ;生成物二氧化碳中含氧元素的质量为
;生成物二氧化碳中含氧元素的质量为![]() ,含碳元素的质量为
,含碳元素的质量为![]() ,则物质X一定含有碳、氧元素,且碳元素的质量为12g-6g=6g,氧元素的质量为
,则物质X一定含有碳、氧元素,且碳元素的质量为12g-6g=6g,氧元素的质量为![]() ,设物质X的化学式为CnOm,碳元素与氧元素的质量比为
,设物质X的化学式为CnOm,碳元素与氧元素的质量比为![]() ,解得n:m=1:1,则物质X为一氧化碳,且一氧化碳的质量为6g+8g=14g,设该一氧化碳完全燃烧生成二氧化碳,需要氧气的质量为x,
,解得n:m=1:1,则物质X为一氧化碳,且一氧化碳的质量为6g+8g=14g,设该一氧化碳完全燃烧生成二氧化碳,需要氧气的质量为x,
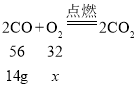
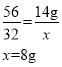
故若起始时增加8g氧气,则无X生成,符合题意。故选D。

 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案【题目】下表是Ca(OH)2和NaOH的溶解度数据。请回答下列问题:
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度/g | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
NaOH | 31 | 91 | 111 | 129 | 313 | 336 | |
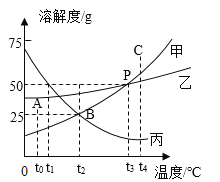
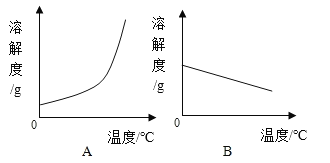
(1)依据上表数据,绘制Ca(OH)2和NaOH的溶解度曲线,下图中能表示NaOH溶解度曲线的是_____(填A或B)。
(2)要想把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,具体措施有:
①加入氢氧化钙,②升高温度,③降低温度,④加入水,⑤蒸发水后再恢复到原温度,⑥加入生石灰。其中措施正确的是_____。
A ②④⑥ B ③④ C ①③⑤⑥ D ①②⑤⑥
(3)20℃时,191g饱和NaOH溶液,蒸发10g水后,再降温到20℃,可析出NaOH晶体的质量为_____。
(4)现有20℃时Ca(OH)2的饱和溶液(甲溶液),向其中加入一定量CaO后得到的溶液(乙溶液),此时溶液中溶质的质量分数乙_____甲(填“>”、“<”或“=”)。
(5)现有60℃时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH晶体,应采取的物理方法是_____。