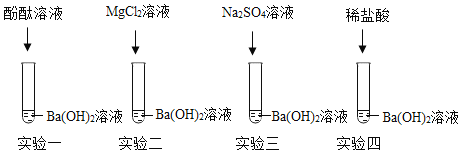
题目内容
【题目】将铜、锌混合物放入一定量的硝酸银溶液中,充分反应后过滤,得到固体和蓝色滤液。
(1)请用化学方程式来解释溶液变为蓝色的原因____。
(2)滤液中溶质有两种可能,猜想一是滤液中含硝酸锌、硝酸铜,请写出第二种猜想中溶质的成分____。
【答案】![]() 硝酸锌、硝酸铜、硝酸银。
硝酸锌、硝酸铜、硝酸银。
【解析】
将铜锌混合物放入一定量的硝酸银溶液中,锌先和硝酸银反应生成硝酸锌和银,铜后和硝酸银反应生成硝酸铜和银。
(1)溶液变为蓝色,是因为铜和硝酸银反应生成硝酸铜和银,反应的化学方程式为:Cu+2AgNO3=Cu(NO3)2+2Ag。
(2)反应后得到固体和蓝色滤液,说明铜已经和硝酸银反应,可能存在硝酸银有剩余,完全反应两种情况。滤液中溶质有两种可能,猜想一是硝酸银完全反应:滤液中含硝酸锌、硝酸铜;
猜想二是硝酸银部分反应:滤液中含有硝酸锌、硝酸铜、硝酸银,这是因为硝酸银过量,则滤液中含有锌、铜和硝酸银反应生成的硝酸锌、硝酸铜和过量的硝酸银。

【题目】一种“环保石头纸”开始被人们使用,其主要成分是碳酸钙。某班同学对它产生了浓厚的兴趣把“环保石头纸”带到实验室,完成了如图所示两个实验。请回答下列问题:
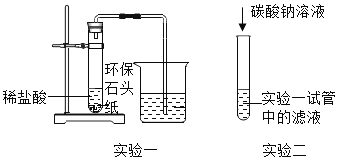
(1)实验一:试管中产生大量的气泡,烧杯中澄清的石灰水变浑浊,请写出“环保石头纸”与稀盐酸发生的反应的化学方程式____(假设“环保石头纸”中的其他的成分既不溶于水,又不与盐酸反应)。
(2)实验二:试管中有白色沉淀产生。小刚同学想探究该实验反应后溶液中溶质的成分。
提出猜想:
猜想Ⅰ:NaCl、CaCl2和HCl;猜想Ⅱ:NaCl和CaCl2;猜想Ⅲ:_____
同学们经过讨论排除了猜想____,理由是_____
有同学认为小刚的猜想不全面,又提出猜想Ⅳ:NaCl和Na2CO3,并通过实验验证了该猜想成立。请你将实验报告补充完整。
实验操作 | 实验现象 | 实验结论 |
取实验二反应后的上层清液少量于试管中,滴加少量____ | ______ | 猜想Ⅳ成立 |
(3)实验结束后,未经处理的废液_____(填“能”或“不能”)直接倒入下水道。