题目内容
【题目】学校研究性学习小组为了测定当地矿山石灰石中碳酸钙的质量分数,取来了一些矿石样品,并取稀盐酸200 g,平均分成4份进行实验,结果如下:
实 验 | 一 | 二 | 三 | 四 |
加入样品的质量/g | 5 | 10 | 15 | 20 |
生成CO2的质量/g | 1.76 | 3.52 | 4.4 | m |
(1)上表中m的数值是________;
(2)反应中矿石有剩余是第_______次实验;
(3)这种石灰石矿中碳酸钙的相对分子质量是_______;
(4)15g碳酸钙中各元素质量比是_______;
(5)求稀盐酸中溶质的质量分数____。(写出计算过程)
【答案】4.4 三、四 100 10:3:12 14.6%。
【解析】
(1)根据表中数据可知,当石灰石质量为15g时,就因50g稀盐酸量不足而石灰石没完全反应,所以,石灰石增加到20g时,50g稀盐酸依然量不足,所以此时产生二氧化碳的质量仍然为4.4g;
(2)第三次实验50g稀盐酸量不足石灰石没完全反应,第四次实验石灰石增加到20g时,50g稀盐酸依然量不足而石灰石没有完全反应,故反应中矿石有剩余是第三、四次实验;
(3)碳酸钙的化学式为CaCO3,故其相对分子质量是:40+12+16×3=100;
(4)碳酸钙中钙、碳、氧元素质量比为:40:12:(16×3)=40:12:48=10:3:12;
此比值与物质的质量无关,故15g碳酸钙中各元素质量比是:10:3:12;
(5)根据表中数据,50g稀盐酸完全反应时生成4.4g二氧化碳,50g稀盐酸中溶质质量为x,

![]() , x=7.3g
, x=7.3g
稀盐酸中溶质的质量分数为:![]() =14.6%
=14.6%

【题目】如图所示图像中,能正确反映对应变化关系的是
A | B | C | D |
|
|
|
|
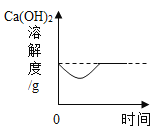
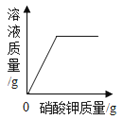
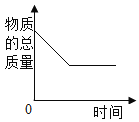
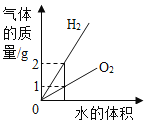
向饱和石灰水中加入一定量CaO | 一定温下,向不饱和硝酸钾溶液中加入硝酸钾固体 | 一定质量的红磷在密闭容器内燃烧 | 电解水生成氢气和氧气质量 |
A. A B. B C. C D. D
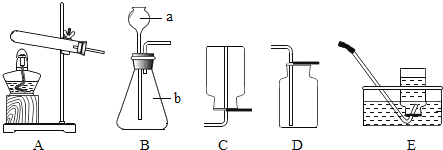
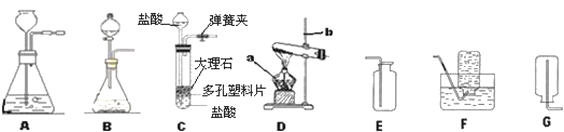
【题目】根据下图回答问题
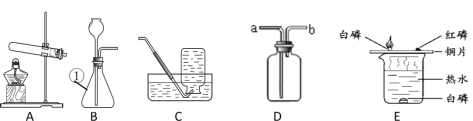
(1)仪器①的名称是__________。
(2)B与C连接制取气体,反应的化学方程式为________。
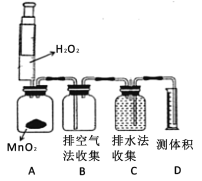
(3)实验室需少量甲烷气,可用加热无水醋酸钠与碱石灰的固体混合物制得。制甲烷气的发生装置应选用____(填字母)装置;收集甲烷气可选用C装置,由此推断甲烷气具有的物理性质是_______。
(4)用图D的装置排水法收集氧气。瓶中装入水的量应为___(选:“少量”、“多量”或“满瓶”),进气口为____(选“a”或“b”)。
(5)E装置用来探究燃烧的条件,由铜片上白磷燃烧而红磷不燃烧得出的结论______。
(6)在实验室制取二氧化碳的研究中,进行了如下实验:
药品 | 甲 | 乙 | 丙 | 丁 |
大理石 | 2g,块状 | 2g,块状 | 2g,粉末状 | 2g,粉末状 |
盐酸(过量) | 20g,10%盐酸 | 20g,20%盐酸 | 20g,10%盐酸 | 20g,20%盐酸 |
Ⅰ、若要研究盐酸浓度大小对反应的影响,可选择实验甲与______对照(选填实验编号)。
Ⅱ、研究发现酸的浓度越大,产生气体的速度越快,与甲比较,对丁分析正确的是_____(填字母序号)
①反应更为剧烈 ②最终剩余溶液的质量更小
③产生的二氧化碳的质量更大 ④粉末状大理石利用率更高
A.① B.①④ C.①③④ D.①②③④