题目内容
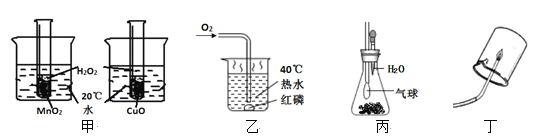
【题目】实验课,同学们利用下列装置进行气体制备的学习。请你用已学的化学知识回答下列问题:
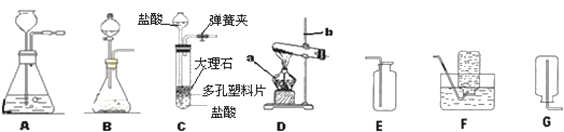
(1)图中仪器a的名称是 __________;
(2)在实验室里常用稀盐酸和块状大理石在装置A中反应制取二氧化碳,收集二氧化碳的装置是:___不用粉末状大理石的原因是_______,写出上述反应化学方程式____________。
(3)装置A、B和C都能制取二氧化碳气体,但装置C与前两者相比较,你认为装置C的优势是_____________。
(4)实验室用加热无水乙酸钠固体和氢氧化钠固体制取甲烷气体.在通常情况下甲烷是一种无色无味的气体,难溶于水,密度比空气小。现实验室制取较纯净的甲烷应选用的装置的组合是_________(填字母编号)。
(5)某同学设计如图装置制取和收集氧气(向上排空气法和排水法),再进行相关实验。A瓶中发生反应的方程式为__________,滴入过氧化氢溶液,观察到A瓶中有气泡产生,C瓶中液面平稳下降,当C瓶中水正好排尽时,取出集气瓶B和C,盖上玻璃片。该同学应选择集气瓶_____(填“B”或 “C”)用于铁丝燃烧实验,另一瓶不合适的具体原因是_____________。
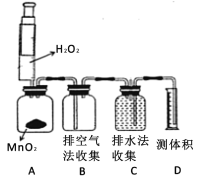
(6)若用氯酸钾和二氧化锰的混合物制氧气,反应的化学方程式为 ________反应前后二氧化锰在固体混合物中质量分数是_________ (“不变”或“变大”或“变小”)。
【答案】酒精灯 E 粉末碳酸钙和盐酸接触面积大,反应较快,气体不好收集,(或反应速率太快不易控制反应进行,不便于实验操作) CaCO3+2HCl═CaCl2+CO2↑+H2O 能使反应随开随用,随关随停(或随时使反应发生,随时使反应停止) D F 2H2O2 ![]() 2H2O+O2↑ C 易导致因高温生成物溅落,使集气瓶底炸裂 2KClO3
2H2O+O2↑ C 易导致因高温生成物溅落,使集气瓶底炸裂 2KClO3![]() 2KCl+3O2↑ 变大
2KCl+3O2↑ 变大
【解析】
(1)图中仪器a的名称是酒精灯;
(2)在实验室里常用稀盐酸和块状大理石在装置A中反应制取二氧化碳,由于二氧化碳的密度比空气的大,收集二氧化碳的装置是E,不用粉末状大理石的原因是粉末碳酸钙和盐酸接触面积大,反应较快,气体不好收集,(或反应速率太快不易控制反应进行,不便于实验操作)所以用大理石固体,碳酸钙和稀盐酸反应生成二氧化碳、氯化钙、水,反应方程式为CaCO3+2HCl═CaCl2+CO2↑+H2O;
(3)比较发现C多一个弹簧夹和隔板,关闭弹簧夹,气体增多压强增大,试管内液面下降,下降到隔板下方后,固体和液体分离,反应停止;打开弹簧夹,气体减少,压强变小,漏斗内液面下降,试管内液面上升,当固体与液体接触时,反应开始。即C的优点是能使反应随开随用,随关随停(或随时使反应发生,随时使反应停止);
(4)实验室用加热无水乙酸钠固体和氢氧化钠固体制取甲烷气体,发生装置属于固体和固体加热制气体;甲烷不溶于水,可以采用排水法收集,实验室制取较纯净的甲烷应选用的装置的组合是D F;
(5)过氧化氢在二氧化锰的作用下分解生成水和氧气,发生反应的方程式为2H2O2 ![]() 2H2O+O2↑,铁在氧气中燃烧时火星四射,放出大量热。应选择集气瓶C,用于铁丝燃烧实验,另一瓶不合适的具体原因是集气瓶底没有水,易导致因高温生成物溅落,使集气瓶底炸裂;
2H2O+O2↑,铁在氧气中燃烧时火星四射,放出大量热。应选择集气瓶C,用于铁丝燃烧实验,另一瓶不合适的具体原因是集气瓶底没有水,易导致因高温生成物溅落,使集气瓶底炸裂;
(6)氯酸钾在二氧化锰的作用下受热分解生成氧气、氯化钾,反应的化学方程式为2KClO3![]() 2KCl+3O2↑,二氧化锰的质量不变,但是反应后固体的质量减少,反应前后二氧化锰在固体混合物中质量分数是变大。
2KCl+3O2↑,二氧化锰的质量不变,但是反应后固体的质量减少,反应前后二氧化锰在固体混合物中质量分数是变大。

【题目】学校研究性学习小组为了测定当地矿山石灰石中碳酸钙的质量分数,取来了一些矿石样品,并取稀盐酸200 g,平均分成4份进行实验,结果如下:
实 验 | 一 | 二 | 三 | 四 |
加入样品的质量/g | 5 | 10 | 15 | 20 |
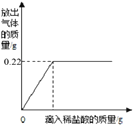
生成CO2的质量/g | 1.76 | 3.52 | 4.4 | m |
(1)上表中m的数值是________;
(2)反应中矿石有剩余是第_______次实验;
(3)这种石灰石矿中碳酸钙的相对分子质量是_______;
(4)15g碳酸钙中各元素质量比是_______;
(5)求稀盐酸中溶质的质量分数____。(写出计算过程)