题目内容
【题目】(10分)人类的生产、生活离不开金属。
(1)目前世界上年产量最高的金属是 (填化学式) ;
(2)铁制品锈蚀,实际上是铁跟空气中的 发生了化学反应。防止铁制栏杆锈蚀的一种方法是 ;
(3)已知下列各组物质间均能发生置换反应。
A.Fe 和CuSO4 溶液 B.Mg和MnSO4 溶液 C.Mn和FeSO4 溶液
①写出Fe 和CuSO4 溶液反应的化学方程式 ;
②Mn、Fe、Mg、Cu四种金属的活动性由强到弱的顺序 。
(4)工业生产中常用10%的稀盐酸来除去铁制品表面的铁锈,实验室若要配制该盐酸200g,则需要溶质的质量分数为38%的浓盐酸 g(计算结果请保留至0.1g);实验室在配制10%的稀盐酸的过程中,除了用到烧杯、量筒和胶头滴管外,还需要用到的玻璃仪器是 。
(5)某化学小组在实验结束后,进行了如下废液处理:
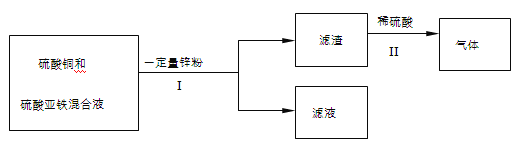
①Ⅰ中的操作名称是 ;
②写出Ⅱ中一定发生反应的化学方程式 ;
③滤液中溶质的组成可能是 (写出一种情况即可)。
【答案】(1)Fe (2)氧气和水蒸气 刷油漆(或镀其他金属 或保持干燥)(3)Fe+CuSO4==FeSO4+Cu ;Mg、Mn、Fe、Cu(4)52.6克;玻璃棒(5)①过滤②Fe+H2SO4 FeSO4+H2↑③硫酸锌
【解析】
试题分析:铁生锈的条件是同时和水分 氧气接触,防锈的措施就是不能同时满足这两个条件,由于提供的三种反应都能发生,Mn和FeSO4 溶液能反应说明Mn的活动性大于Fe,配置溶液的时候还需要玻璃棒,用来搅拌加快溶解,由于是加入一定量的锌粉,没有强调量的多少,所以可能的情况有三种:过量;不足 恰好。当过量时锌粉就能把铜和铁都置换出来,所以溶液中只有硫酸锌。

【题目】(12分)小明同学对“锌与硫酸反应快慢的影响因素”进行了探究。
【提出问题】锌与硫酸反应的快慢受哪些因素的影响呢?
【猜想与假设】
a.可能与硫酸的质量分数有关;
b.可能与锌的形状有关。
【查阅资料】
锌的化学性质比较活泼,在常温下的空气中,表面生成一层“保护膜”,可阻止进一步氧化。该“保护膜”可以和酸反应,但不产生氢气。
【设计并实验】小兵用不同质量分数的硫酸和不同形状的锌进行如下实验。
实验编号 | 硫酸的质量分数(均取20mL) | 锌的形状(均取1g) | 氢气的体积(mL)(均收集3分钟) |
① | 20% | 锌粒 | 31.7 |
② | 20% | 锌片 | 50.9 |
③ | 20% | 锌粒 | 61.7 |
④ | 30% | 锌片 | 79.9 |
(1)写出稀硫酸与锌反应的化学方程式______________________________。
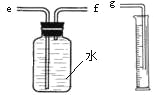
(2)小兵用图装置收集并测量氢气的体积,其中量筒的作用是_______________________,
氢气应从________(填e或f或g)管通入;
【收集证据】
(3)要比较不同质量分数的硫酸对反应快慢的影响,应选择的实验编号是____________;
【得出结论】
(4)结论是_____________________________________________________;
【评价与反思】
(5)下表是小兵第①组实验的详细数据。
时段(均为1分钟) | 第1分钟 | 第2分钟 | 第3分钟 | 第4分钟 | 第5分钟 | 第6分钟 |
H2的体积 | 3.1mL | 16.7mL | 11. 9mL | 9.6mL | 7.6mL | 6.0mL |
请描述锌与硫酸反应的先慢后快最后又变慢的原因___________________________;
(6)你认为锌与硫酸反应的快慢可能还受 因素影响?
(7)取某厂生产的生铁样品6g,与100g足量的稀硫酸充分反应后,称得剩余物质的总质量为105.8g。
①生成气体的质量为 克;
②该厂生产的生铁样品中铁的质量分数是多少?(写出具体的过程,结果精确到0.1%)
③该厂生产的生铁是否合格? (填“合格”或“不合格”)