题目内容
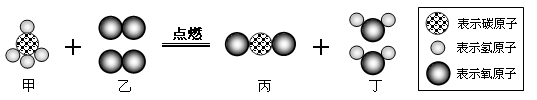
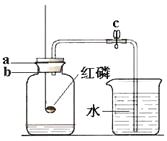
【题目】用来测定空气成分的方法很多,下图所示的是小明用红磷在空气中燃烧的测定方法。

实验过程是:
第一步:将集气瓶容积划分为五等份,并做好标记。
第二步:点燃燃烧匙内的红磷,伸入集气瓶中并把塞子塞紧。
第三步:待红磷熄灭并冷却后,打开弹簧夹,发现水被吸入集气瓶中,进入集气瓶中水的体积约为集气瓶总容积的1/5。
请回答下列问题:
(1)上面的实验同时证明了氮气有 的化学性质。
(2)实验完毕,若进入集气瓶中水的体积不到总容积的1/5,你认为导致这一结果的原因可能 。
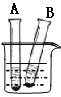
(3)某同学对实验进行反思后,提出了改进方法(如图所示),

你认为改进后的优点是: 。
【答案】(1)不能燃烧,也不支持燃烧 (2)装置漏气 或 红磷的量不足
(3)装置始终密闭,空气没有逸出,实验结果准确
【解析】
试题分析:(1)红磷燃烧消耗完氧气后会熄灭,说明氮气有不能燃烧,也不支持燃烧的化学性质
(2)若进入集气瓶中水的体积不到总容积的1/5,可能原因:装置漏气、红磷的量不足、未冷却至室温就打开止水夹,使进入瓶内水的体积减少,
(3)改进后的实验优点是:装置始终密闭,空气没有逸出,实验结果准确

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目