题目内容
【题目】下列做法,能达到实验目的是![]()
A. 用铁丝代替红磷,粗略地测定空气中氧气的含量
B. 用25mL蒸馏水和25mL酒精配制50mL酒精溶液
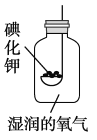
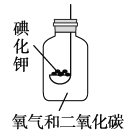
C. 将气体通入足量氢氧化钠溶液,除去![]() 中少量的CO
中少量的CO
D. 将稀硫酸滴在金属表面,鉴别真黄金和假黄金![]() 铜锌合金
铜锌合金![]()
【答案】D
【解析】A、铁丝在空气中不能燃烧,不能用于粗略地测定空气中氧气的含量,不能达到实验目的,错误;B、分子之间有间隔,一部分水分子和酒精分子会互相占据分子之间的间隔,用25mL蒸馏水和25mL酒精混合,所得酒精溶液小于50mL,不能达到实验目的,错误;C、CO2能与氢氧化钠溶液反应生成碳酸钠和水,CO不与氢氧化钠溶液反应,反而会把原物质除去,不符合除杂原则,不能达到实验目的,错误;D、真黄金不能与稀硫酸反应,假黄金中的锌能与稀硫酸反应生成氢气,故分别将稀硫酸滴在金属表面,有气泡产生的是假黄金(铜锌合金),没有气泡产生的是真黄金,能达到实验目的,正确。故选D。

 名校课堂系列答案
名校课堂系列答案【题目】同学们可以通过下列方式认识空气。
【组成角度】
①空气中体积分数约为78%的物质是___________。
②为测定空气中氧气体积分数,设计下图实验。
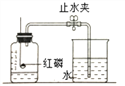
Ⅰ.为了确保实验成功,在装药品之前应该检查装置的 _________;
Ⅱ.该实验中红磷需要过量的原因是__________;
Ⅲ.红磷燃烧的现象是____________,反应的化学方程式 ____________;
Ⅳ.冷却至室温后打开止水夹观察到的现象是 _______________;由此得出空气中氧气的体积分数约为 ___________。
【微观角度 】
①用“化学符号”或“图示”填空。
![]()
图 示 |
| ______ |
|
化学符号 | ______ | N2 | _______ |
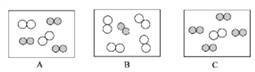
②同温同压下,气体的体积比等于分子个数比。若忽略空气中其它成分,如图可表示空气微观模型的是__________(填选项)。
【变化角度】
在一个标准大气压下,空气中部分组分的沸点如下:
组分 | 氮气 | 氧气 | 二氧化碳 |
沸点(℃) | -195.8 | -183.0 | -78.4 |
①将燃着的木条置于盛有表中组分的混合液的钢瓶口,观察到的现象是____________。
②下列叙述错误的是_____________。
A.木炭在氧气中燃烧,发出白光
B.铁丝在空气中燃烧,火星四射,生成黑色固体
C.从冰箱里拿出汽水,瓶子外表有液珠,说明空气中有水蒸气
D.久置澄清石灰水的试剂瓶内壁有一层白膜,证明空气中有二氧化碳
③铁丝在氧气中燃烧的化学方程式是____________。
【应用角度】
①酒精(C2H5OH)是一种常用消毒剂,酒精由___________种元素组成,其中氢元素与氧元素的质量比为_______;氢元素的质量分数为________(可用分数表示);每个酒精分子含________个原子;46gC2H5OH中含_________个氧原子。配平酒精燃烧的化学方程式的系数依次为_______。
□C2H5OH+□O2![]() □CO2+□H2O
□CO2+□H2O
②食品包装内充N2以防腐,因为N2的化学性质_____________;
【题目】今天老师拿来两瓶无标签的试剂,一瓶是固体一瓶是液体。老师将二者取少量混合在试管里,便产生了一种无色气体。我们对气体进行了多种探究。
(1)①该气体是那种物质?验证它的方案如下:
猜 想 | 试 验 步 骤 | 现 象 及 结 论 |
此气体可能是__________ | ________________ | ______________ |
产生该气体的化学方程式可能是____________________________________
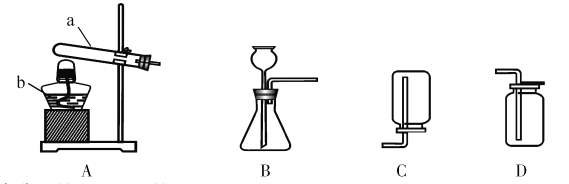
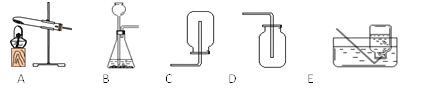
②我想制取该气体,采用的发生装置可选用下图中的_____,收集装置是____。(2)我猜想该无色气体还可能是另一种气体,制取该气体的化学方程式是_____________________________。
(3)实验室可用熟石灰和氯化铵两种固体加热反应制取氨气,氨气是一种极易溶于水、密度比空气小的气体。根据以上所述,实验室制取氨气应该选用的发生装置是_________,收集装置选用__________。
【题目】下表是氢氧化钙和氢氧化钠的溶解度数据。请回答下列问题:
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度 (g/100gH2O) | 氢氧化钙 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
氢氧化钠 | 31 | 91 | 111 | 129 | 313 | 336 | |
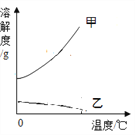
① 氢氧化钠溶解度曲线是____(选填“甲”或“乙”)
② 把接近饱和的氢氧化钙溶液变成饱和溶液的方法是______。
③ 20 ℃时,10 g水中溶解______克氢氧化钠恰好饱和。
④ 20 ℃时,分别在100克水中加入m克氢氧化钠和氢氧化钙固体,可得到质量分数相同的两种溶液,则m的取值范围是______。
⑤ 60 ℃时,氢氧化钠的饱和溶液中含少量氢氧化钙,把其降温,结晶后过滤,对滤渣、滤液成分分析正确的是______。
Ⅰ.滤渣中只有氢氧化钠
Ⅱ.滤渣中一定有氢氧化钠,可能有氢氧化钙
Ⅲ.滤液中一定有氢氧化钙,可能有氢氧化钠
Ⅳ.滤液中一定有氢氧化钠和氢氧化钙
⑥ 氢氧化钙溶液和氢氧化钠溶液都是无色溶液,都能与二氧化碳发生反应。氢氧化钠与二氧化碳反应的方程式为: 2NaOH + CO2![]() Na2CO3+H2O。氢氧化钙与二氧化碳反应的方程式为______________。
Na2CO3+H2O。氢氧化钙与二氧化碳反应的方程式为______________。
根据以上信息,你认为____(选填“能”或“不能”)用二氧化碳来鉴别这两种溶液。