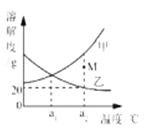
题目内容
【题目】(1)化学小组选用下图装置制取并收集氧气。
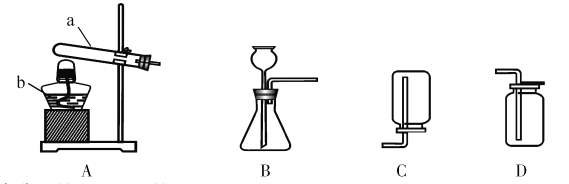
①仪器的名称:a是______,b是______。
②实验事制取氧气的化学方程式为______(写一个),实验时对应的气体发生和收集装置分别是______(填标号,下同)和______。
(2)碘化钾(KI)足白色固体,保存不当会被氧化为单质碘(I2)而泛黄变质。化学小组查得以下资料:
I.对于碘化钾变质的原理,有两种不同的反应:
甲:4KI+O2+2CO2= 2K2CO3+2I2
乙:4KI+O2+2H2O=4KOH+2I2
Ⅱ.KOH与NaOH的化学性质相似。
为探究碘化钾变质原理的合理性,开展以下实验。
【实验过程】
[实验1]
取适量碘化钾固体暴露于空气小一段时间,观察到固体泛黄。往泛黄的固体中加入足量稀硫酸,产生无色无味的气体,通入澄清石灰水中,澄清石灰水变浑浊。
①石灰水变浑浊的原冈是______(用化学方程式表示)。
②化学小组认为:据此现象,还不能得出“反应甲是造成碘化钾变质的原因”的结论。理由是____。
[实验2]
按右上图所示装置进行实验,数日后,观察到碘化钾固体无泛黄现象。
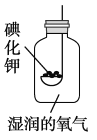
③据此现象,可得出的结论是______。
[实验3]
按右下图所示装置进行实验,数日后,观察到碘化钾同体无泛黄现象。
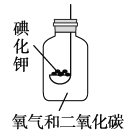
查阅文献获知,常温下某些气体和固体反应须在潮湿环境中进行。化学小组据此改进实验,很快观察到固体泛黄的现象。
④简述化学小组改进实验的具体措施:___________。
【实验结论】
⑤根据上述实验,化学小组得出结论:碘化钾固体泛黄变质是碘化钾与_____共同作用的结果。
【答案】(1)①试管 酒精灯
②2KMnO4![]() K2MnO4+MnO2+ O2↑(或“2H2O2
K2MnO4+MnO2+ O2↑(或“2H2O2![]() 2H2O+O2↑”等其他合理答案);
2H2O+O2↑”等其他合理答案);
A(或“B”)D
(2)①CO2+Ca(OH)2=CaCO3↓+H2O
②无法判断K2CO3是按反应甲原理产生,还是按反应乙原理生成的KOH吸收空气中的CO2而产生的(或其他合理答案)
③反应乙不是造成碘化钾泛黄的原因(或其他合理答案)
④往瓶中再加入少量水(或其他舍理答案)
⑤氧气、水和二氧化碳
【解析】(1)①由图可知,a是试管,b是酒精灯;②实验室制取氧气的方法有三种:分解过氧化氢、加热高锰酸钾、加热氯酸钾,其中加热高锰酸钾分解制取氧气的同时,还生成了锰酸钾和二氧化锰,故反应的化学方程式是2KMnO4 △K2MnO4 +MnO2 + O2↑;用加热高锰酸钾制取氧气属固固加热型,发生装置选A;氧气的密度比空气大,难溶于水,可用向上排空气法或排水法收集,收集装置选D;(2)①澄清石灰水的主要成分是氢氧化钙,二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,反应的化学方程式表示为CO2+Ca(OH)2=CaCO3↓+H2O;②由于氢氧化钾易与空气中的二氧化碳反应生成碳酸钾,故不能判断反应生成的碳酸钾是按反应甲原理产生,还是按反应乙原理生成的;③由实验图示可知,该实验提供的反应物碘化钾、水和氧气,故反应乙不是造成碘化钾泛黄的原因;④根据资料“常温下某些气体和固体反应须在潮湿环境中进行”,故可往瓶中再加入少量水进行改进;⑤根据实验可知,碘化钾固体泛黄变质是碘化钾与氧气、水和二氧化碳共同作用的结果。