题目内容
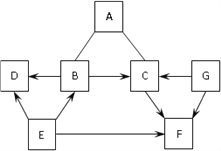
【题目】图中A、B、C、D是四种粒子的结构示意图,请回答下列问题:
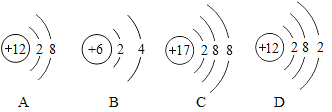
(1)图中A、B、C、D粒子共表示___种元素。
(2)A、B、C、D中的阳离子与阴离子所形成的化合物的化学式为____。
(3)晶体硅是制造半导体芯片的原料,如图是硅原子的结构示意图,图中x的值是____,硅与氧元素组成SiO2,写出该物质名称____。
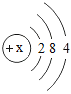
(4)硅元素的化学性质与A、B、C、D中___(填字母序号)对应的元素的化学性质相似。
【答案】3 MgCl2 14 二氧化硅 B
【解析】
(1)图中A、B、C、D粒子共表示3种元素,因为其中的质子数有三种,分别是6,12,17,故填:3。
(2)A、B、C、D中的阳离子与阴离子所形成的化合物的化学式为MgCl2,因为其中的阳离子是镁离子,阴离子是氯离子,所以形成的化合物是氯化镁,故填:MgCl2。
(3)晶体硅是制造半导体芯片的原料,如图是硅原子的结构示意图,根据原子中质子数=核外电子数,所以图中x的值是14,硅与氧元素组成SiO2,该物质名称为二氧化硅,故填:14 二氧化硅;
(4)硅元素的化学性质与A、B、C、D中B对应的元素的化学性质相似,因为它们的原子的最外层电子数都是4,最外层电子数相同的原子化学性质相似,故填:B。

【题目】氯化钠与硝酸钠的溶解度曲线如图:
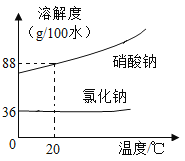
(1)20℃时溶解度较小的物质是______。
(2)从硝酸钠和氯化钠的混合溶液中提纯硝酸钠的方法是_____,可以利用该方法提纯硝酸钠的理由是_____。
Ⅰ.固体混合物中硝酸钠的含量较高,氯化钠的含量较低
Ⅱ.硝酸钠的溶解度受温度影响变化较大
Ⅲ.0℃至100℃,硝酸钠的溶解度始终大于氯化钠
(3)海水中有氯化钠,我们可以利用海水晒盐。某地海水中主要物质的含量见表。
物质 | 每100g海水所含质量(g) |
水 | 96.5 |
氯化钠 | 2.7 |
硫酸钠 | 0.2 |
…… |
①该海水中氯化钠的质量分数为_____。
②20℃时的100g该海水,当水的蒸发量大于____g时,开始析出氯化钠。