题目内容
【题目】某研究性学习小组用如图所示装置进行如下实验(不考虑气体与水或盐的反应)。
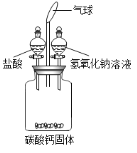
(1)先向广口瓶中加入一定量盐酸溶液,关闭活塞,震荡,观察到固体全部溶解,气球变大。然后再将一定量氢氧化钠溶液加入广口瓶中,关闭活塞,震荡,发现气球明显变小,同时在广口瓶中还能观察到的现象是___________________, 用化学方程式表示该现象产生的原因:_____________________________________。
(2)实验结束后,同学们对广口瓶中的溶液进行探究。
(提出问题)广口瓶中的溶液含有哪些溶质?
(交流讨论)小明取广口瓶中溶液少量加入试管内,向其广口瓶中加入过量稀盐酸,发现有气泡产生,由此他得出结论:广口瓶中溶液的溶质组成为Na2CO3、NaCl、CaCl2。大家一致认为小明的结论是不正确的,理由是________________________________。后经大家讨论,达成共识,对广口瓶溶液中溶质组成的判断只有两种结论,结论一:组成为__________________________两种溶质,结论二:组成为____________________________________ 三种溶质。
(3)(实验设计)
实验步骤 | 实验现象 | 实验结论 |
①取广口瓶中溶液少量于试管中,向其中加入过量的________溶液 | 有白色沉淀产生 | 结论一是正确的 |
②向步骤①所得的溶液中加______________ | ______________ |
反思讨论:第①步加入试剂要求过量的作用是:________________________________________________。
【答案】有白色沉淀产生 CaCl2+Na2CO3=CaCO3↓+2NaCl 碳酸钠能与氯化钙反应生成碳酸钙沉淀,二者不能共存 Na2CO3、NaCl NaOH、NaCl、Na2CO3 氯化钙(CaCl2) 酚酞试液 溶液无明显颜色变化 验证并除去碳酸根离子
【解析】
(1)同时在广口瓶中还能观察到产生白色沉淀,是因为碳酸钠和氯化钙反应生成白色沉淀碳酸钙和氯化钠,反应的化学方程式:Na2CO3+CaCl2═CaCO3↓+2NaCl。
(2)结论是不正确的,理由是碳酸钠和氯化钙反应生成碳酸钙沉淀,两者不能共存;
后经大家讨论,达成共识,对广口瓶溶液中溶质组成的判断只有两种结论,结论一:组成为碳酸钠、氯化钠两种溶质,结论二:组成为碳酸钠、氯化钠、氢氧化钠三种溶质。
(3)①取广口瓶中溶液少量于试管中,向其中加入过量的氯化钙溶液,产生白色沉淀,是因为碳酸钠和氯化钙反应生成了白色沉淀碳酸钙,说明溶液中含有碳酸钠。
②向步骤①所得的溶液中加酚酞试液,酚酞试液不变色,说明溶液中不含有氢氧化钠,说明结论一是正确的。
反思讨论:第①步加入试剂要求过量的作用是验证并除去碳酸根离子,以防止对检验氢氧根离子产生影响。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】2018年春节南昌市出台了禁止燃放烟花爆竹的规定。针对烟花爆竹燃放产生的气体成分,化学兴趣小组同学展开了如下探究:
(提出问题)烟花爆竹燃烧后生成哪些气体?
(查阅资料)
(1)爆竹的主要成分是黑火药,含有硫磺、木炭粉、硝酸钾。
(2)SO2易溶于水,化学性质与二氧化碳有相似之处,它能使澄清石灰水变浑浊,生成CaSO3,将SO2气体通入紫红色的酸性高锰酸钾溶液中,溶液会褪色。
(提出猜想)猜想1:CO2 猜想2:SO2 猜想3:CO2和SO2
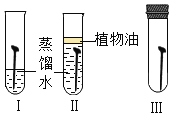
(实验探究)兴趣小组同学合作设计了如下实验装置,验证猜想的气体。
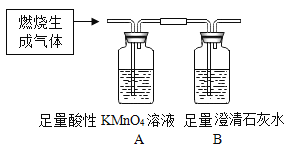
(现象与结论)
现象 | 结论 |
①装置A中溶液不褪色,装置B中石灰水变浑浊 | 猜想1成立 |
②装置A中_____,装置B中______ | 猜想2成立 |
③装置A中_____,装置B中______ | 猜想3成立 |
(反思评价)兴趣小组经讨论认为A、B装置的顺序不能颠倒,其原因是____。
A 不能确定含有CO2
B 不能确定含有SO2
C 不能确定含CO2和SO2
(思维拓展)集中燃放烟花爆竹对环境造成相当严重的污染,这些污染主要是:_____________。
【题目】归纳、整理是学习化学的有效方法。下列选项正确的是( )
A.认识化学式 “珍惜生命,远离毒品”某毒品化学式为C12H10O2N,该物质由四种元素组成;该物质由25个原子构成 | B.性质决定用途 石墨具有良好的导电性——可作电极 氧气具有助燃性——可作燃料 |
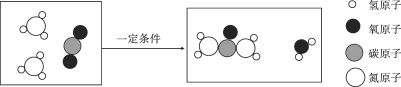
C.理解化学方程式 2H2O | D.化学与能源 化石燃料属于不可再生能源; 太阳能、风能、氢能属于清洁能源 |
A.AB.BC.CD.D
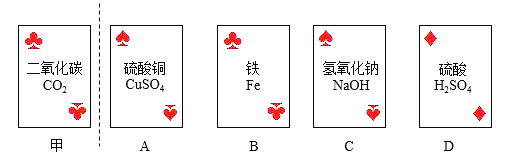
【题目】分类、类比和总结是初中化学常用的学习方法。
(1)初中化学实验可按实验目的分为:探究物质的性质,探究物质的含量,探究反应的条件等,根据实验目的,可将实验_____(填字母)分为一类;分类的依据是_____。
|
|
|
|
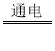
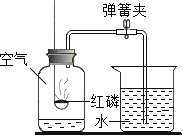
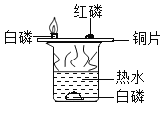
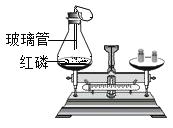
A.测定空气中氧气的含量 | B.探究可燃物燃烧的条件 | C.探究反应前后物质的质量关系 | D.探究铁钉生锈的条件 |
(2)工业上可用电解饱和氯化钠溶液制取氢氧化钠,同时还能生成两种气体单质,生成的两种气体在点燃的条件下反应会生成制盐酸的气体,请写出上述制取氢氧化钠的化学方程式:_____;此反应前后化合价发生改变的元素为_____(填元素符号)。