题目内容
【题目】勇往直前学习小组的同学们在实验室中探究“碱的化学性质”,请你参与!
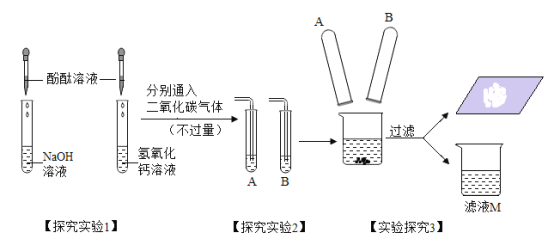
(探究实验 1)实验中观察到 A、B 试管内出现的现象为______________________。
(探究实验 2)B 试管中发生反应的化学方程式为_____________________________, 此反应在生活中的一个应用是______________________________________________。
结合上述实验及你所了解的氢氧化钠的性质,分析氢氧化钠必须密封保存的原因_______________。
(探究实验 3)同学们对所得到的滤液 M 中的离子组成展开探究:
(提出问题)滤液 M 中含有哪些离子?
(猜想假设)小冰的猜想:Na +、OH -
小城的猜想:Na +、OH -、CO3 2-
小美的猜想:Na +、CO3 2-
小丽的猜想: _______(填离子符号)
(设计实验)为了验证自己的猜想是正确的,小城取适量滤液 M 于试管中,向其中滴加过量氯化钙溶液,观察到_____________,则可以证明自己的猜想是正确的。
(拓展延伸)为科学处理剩余的滤液 M,可以进行的操作是____________________________,就可以排放了。 同学们成功地完成了探究,在探究过程中体现了他们严谨认真的科学精神,对废液的合理处理更体现了他们高度的社会责任感。这是非常值得我们学习的。
【答案】溶液变红 ![]() 粉刷墙壁 氢氧化钠能与空气中的二氧化碳反应变质
粉刷墙壁 氢氧化钠能与空气中的二氧化碳反应变质 ![]() 、
、![]() 、
、![]() 有白色沉淀生成,溶液仍为红色 加入适量稀盐酸使溶液显中性
有白色沉淀生成,溶液仍为红色 加入适量稀盐酸使溶液显中性
【解析】
探究实验 1:
氢氧化钠、氢氧化钙溶液均显碱性,使无色酚酞变红,实验中观察到 A、B 试管内出现的现象为溶液变红。
探究实验 2:
B 试管中氢氧化钙与二氧化碳反应生成碳酸钙沉淀和水,发生反应的化学方程式为![]() ,此反应在生活中的一个应用是粉刷墙壁。
,此反应在生活中的一个应用是粉刷墙壁。
结合上述实验及你所了解的氢氧化钠的性质,分析氢氧化钠必须密封保存的原因是:氢氧化钠能与空气中的二氧化碳反应变质。
探究实验 3:
猜想假设:
小丽的猜想:可能氢氧化钙有剩余,此时,溶液中的离子有![]() 、
、![]() 、
、![]() 。
。
设计实验:
为了验证自己的猜想是正确的,小城取适量滤液 M 于试管中,向其中滴加过量氯化钙溶液,观察到有白色沉淀生成,溶液仍为红色,则可以证明自己的猜想是正确的,因为碳酸钙离子与钙离子结合生成碳酸钙沉淀,氢氧化钠能使酚酞就红色。
拓展延伸:
盐酸能与氢氧化钠、碳酸钠、氢氧化钙反应,生成中性的氯化钠、氯化钙、水和二氧化碳等。为科学处理剩余的滤液 M,可以进行的操作是加入适量稀盐酸使溶液显中性,就可以排放了。

 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案