题目内容
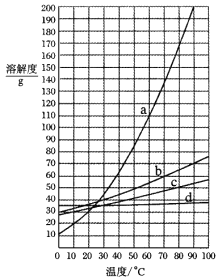
【题目】如图是氢氧化钠溶液和盐酸用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线。

(1)氢氧化钠和盐酸恰好完全反应时,溶液的pH 7(填“大于”“小于”或“等于”)。
(2)根据曲线判断,该反应是将 (填“氢氧化钠溶液”或“盐酸”,下同)滴入 中,理由是 。
(3)当滴入溶液的体积为5 mL时,所得溶液中的溶质为 (写化学式),若在此溶液中滴入石蕊试液,溶液显 色。
【答案】(1)等于
(2)氢氧化钠溶液 盐酸 随着滴入溶液的增加,溶液的pH增大
(3)NaCl和HCl 红
【解析】本题主要考查中和反应、溶液的酸碱性与pH的关系。(1)氢氧化钠和盐酸恰好完全反应时,酸和碱都没有剩余,溶液显中性,pH=7;(2)根据图像,在反应未进行时,溶液的pH=1,为酸性溶液,所以该反应是将氢氧化钠溶液滴入盐酸中;(3)盐酸和氢氧化钠的反应原理是:HCl+NaOH=NaCl+H2O,滴入氢氧化钠溶液的体积为5 mL时,溶液仍为酸性,所以是氢氧化钠只和部分盐酸反应,所得溶液中的溶质有生成的氯化钠也有剩余的盐酸,酸使石蕊显红色。

练习册系列答案
相关题目
【题目】下列实验中,现象与结论对应关系正确的是( )
A | B | C | D | |
图 示 |
|
|
|
|
现 象 | 有大量气泡产生,生成的气体使澄清石灰水变浑浊 | 冷却后,打开弹簧夹,水被吸入瓶内,瓶内水面上升约 1/5 | ①中铁钉生锈, ②③中铁钉不生锈 | 滴加无色酚酞, 溶液呈红色,加入稀盐酸后红色变为无色 |
结论 | 该粉末中一定含有 碳酸钠 | 氧气约占空气质量的1/5 | ①②对比说明铁生锈条件之一是要与水接触 | 反应后的溶液一定不呈 碱性 |
A. A B. B C. C D. D