题目内容
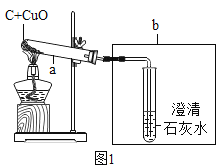
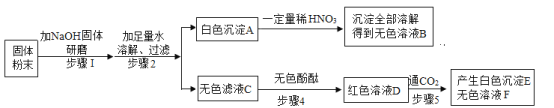
【题目】某干燥剂含有CaO、NaOH和CaCl2中的两种物质。为了探究其成分,设计了如图所示实验。下列说法正确的是( )

A.溶液a形成过程中一定只发生物理变化B.b溶液中一定有NaOH和Na2CO3
C.得到的白色固体一定不是纯净物D.干燥剂一定由 NaOH和CaCl2组成
【答案】B
【解析】
A、氧化钙和水反应生成氢氧化钙,所以溶液a形成过程中也会发生化学变化,故A错误;
B、如果干燥剂中是氢氧化钠和氯化钙时,b溶液中一定有没有反应的氢氧化钠和过量的碳酸钠,如果干燥剂中是氢氧化钠和氧化钙时,氢氧化钠不能反应,氧化钙和水反应生成氢氧化钙,氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,因此b溶液中一定有没有反应的氢氧化钠和反应生成的氢氧化钠和过量的碳酸钠,如果干燥剂中是氧化钙和氯化钙时,氧化钙和水反应生成氢氧化钙,氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,因此b溶液中一定有反应生成的氢氧化钠和过量的碳酸钠,因此无论干燥剂中含有哪两种物质,b溶液中一定有NaOH和Na2CO3,该B正确;
C、白色固体是碳酸钙,属于纯净物,故C错误;
D、由实验现象可知,干燥剂可以是CaO、NaOH和CaCl2中的任意两种物质,故D错误。
故选:B。

 期末1卷素质教育评估卷系列答案
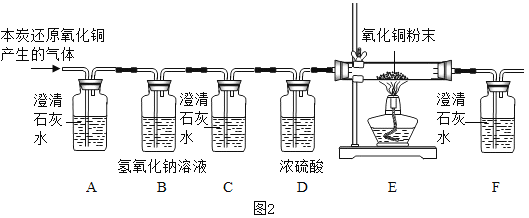
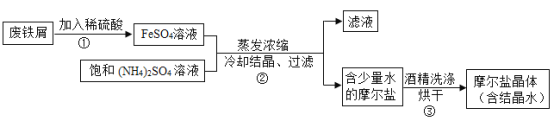
期末1卷素质教育评估卷系列答案【题目】红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示。同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究。

(提出问题)久置固体的成分是什么?
(查阅资料)铁与氯化铁溶液在常温下发生反应生成氯化亚铁。
(作出猜想)久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3。
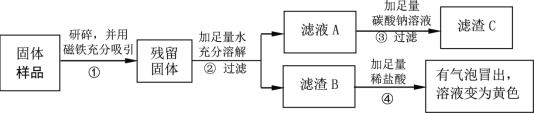
(实验探究1)
甲同学的方案:
实验操作 | 实验现象 | 实验结论 |
(1)取少量固体放于试管中,加足量蒸馏水溶解,静置后取上层清液滴加无色酚酞溶液 | 固体溶解时试管外壁发烫,试管底部有不溶物,溶液变红。 | 固体中一定含有______ |
(2)另取少量固体放于试管中,滴加足量的稀盐酸。 | 固体逐渐消失,有大量无色气体产生,得到浅绿色溶液。 | 固体中一定含有_______, 一定不含Fe2O3 |
(3)将步骤(2)中产生的气体通入到澄清的石灰水中 | 石灰水变浑浊 | 固体中一定含有______ |
(实验质疑)
乙同学认为甲同学的实验并不能得出一定不含Fe2O3的结论,理由是_______。
(实验探究2)
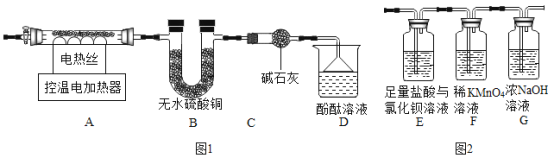
乙同学设计如下实验方案继续验证:
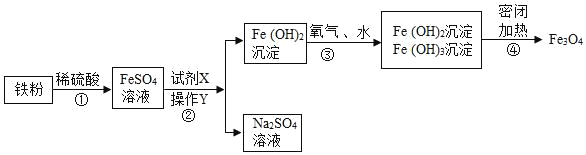
(1)③中反应的化学方程式是______。
(2)乙同学实验中又能得出固体样品中一定还含有______。
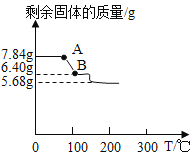
(3)乙同学又经过实验测得上述残留固体中含钙物质的总质量为1.6 g,滤渣B中CaCO3的质量为1.0 g,滤渣C的质量为1.0 g。
(实验结论)综合上述实验及所给数据,久置固体的成分是________。
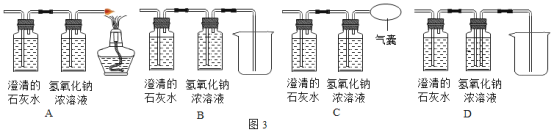
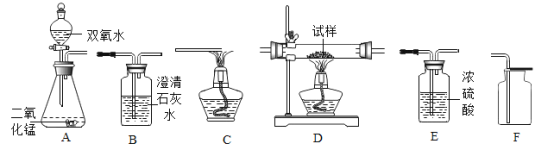
【题目】某化学兴趣小组为“探究纯碱的性质”中,同学们做了如图所示的四组实验,并将A、B、C、D四支试管中反应后的废液全部倒入一个洁净的大烧杯中。一段时间后发现,烧杯上层得到无色澄清的溶液。为了探究该溶液的成分,进行了以下实验。

(提出问题)大烧杯中的上层溶液中除了含有水和酚酞外,还含有哪些物质?
(猜想假设)猜想一:NaCl、BaCl2、CaCl2 猜想二:NaCl、BaCl2、CaCl2、HCl
猜想三:NaCl、BaCl2、CaCl2 、Ca(OH)2 猜想四:NaCl、BaCl2、CaCl2、Na2CO3
(分析讨论)上述猜想中一定错误的是猜想三和_____(填序号),为说明上述的原因,请用一个化学方程式解释为_____。
(设计实验)为进一步确定上层溶液中溶质的成分。另三个同学设计如下实验方案,进行探究:
实验操作 | 实验现象 | 实验结论 |
实验一:取大烧杯中上层溶液少许于一支试管中,滴加少量的石蕊试剂。 | 溶液变成_____色 | 猜想二正确。 |
实验二:取大烧杯中上层溶液少许于一支试管中,逐滴滴加碳酸钠溶液至过量。 | 有气泡产生,并有白色沉淀生成,_____; | 猜想二正确。 |
实验三:取大烧杯中上层溶液少许于一支试管中,滴加少量的硝酸银溶液。 | 产生白色沉淀 | 猜想二正确。 |
(交流讨论)大家讨论后得出,实验三结论是不严谨的,原因是_____。
(实验结论)通过上述探究,猜想二是正确的。