题目内容
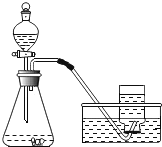
【题目】实验室常用下列装置来制取气体:

(1)在实验室中,甲同学想用高锰酸钾为原料制取一瓶纯净的氧气,他应选择的装置组合是____(填字母编号),写出该反应的符号表达式________________。夏天室温很高的时候,检验装置A气密性的合理方法是:先将导管的一端伸入水中,然后_______________ ,若导管口有气泡冒出,说明装置不漏气。
(2)乙同学用B装置进行实验室制取二氧化碳,应该选择的药品是______ 和____(写名称),发现该装置有一处错误:____________ ,该反应的符号表达式为:_____________。为控制反应的剧烈程度,他还应将B装置中的某仪器改为____________(填仪器名称),如果用F装置收集CO2,则CO2从______端进入(填“a”或“b”)。
(3)通过查阅资料得知:氨气是一种密度比空气小且极易溶于水的气体,其水溶液俗称氨水。小美同学利用加热氯化铵(NH4Cl)固体和氢氧化钙 [Ca(OH)2] 固体生成氯化钙(CaCl2)、氨气和水的方法制取氨气,此反应的符号表达式为_________________________,她可选择的收集装置是_______(填字母编号)。
【答案】AEKMnO4![]() K2MnO4+MnO2+O2酒精灯微热试管 (或热毛巾包捂试管)大理石稀盐酸 长颈漏斗的下端没有伸到液体以下(或长颈漏斗的下端没有形成液封)CaCO3+HCl
K2MnO4+MnO2+O2酒精灯微热试管 (或热毛巾包捂试管)大理石稀盐酸 长颈漏斗的下端没有伸到液体以下(或长颈漏斗的下端没有形成液封)CaCO3+HCl![]() CaCl2+H2O+CO2分液漏斗aNH4Cl+Ca(OH)2
CaCl2+H2O+CO2分液漏斗aNH4Cl+Ca(OH)2![]() CaCl2+NH3+H2O D
CaCl2+NH3+H2O D
【解析】
(1)如果用高锰酸钾制氧气就需要加热,应选择装置A,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,反应的符号表达式:KMnO4![]() K2MnO4+MnO2+O2;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,用排水法收集的氧气比较纯净,应选择装置E;夏天室温很高的时候,检验装置A气密性的合理方法是:将导管口放入水面下,然后酒精灯微微加热或热毛巾包捂,若导管口有气泡冒出,说明装置不漏气;
K2MnO4+MnO2+O2;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,用排水法收集的氧气比较纯净,应选择装置E;夏天室温很高的时候,检验装置A气密性的合理方法是:将导管口放入水面下,然后酒精灯微微加热或热毛巾包捂,若导管口有气泡冒出,说明装置不漏气;
(2)实验室取二氧化碳,应该选择的药品是大理石或石灰石和稀盐酸;该反应的符号表达式为:CaCO3+HCl![]() CaCl2+H2O+CO2;据图可知:该装置中长颈漏斗的下端没有伸到液体以下;控制反应的剧烈程度,他应将B装置中的长颈漏斗改为分液漏斗;如果用F装置收集CO2,由于CO2的密度比空气大,则氧气由a端通入;
CaCl2+H2O+CO2;据图可知:该装置中长颈漏斗的下端没有伸到液体以下;控制反应的剧烈程度,他应将B装置中的长颈漏斗改为分液漏斗;如果用F装置收集CO2,由于CO2的密度比空气大,则氧气由a端通入;
(3)加热氯化铵和氢氧化钙固体混合物的方法制取氨气,同时生成氯化钙和水,其反应的符号表达式为:NH4Cl+Ca(OH)2![]() CaCl2+NH3+H2O;氨气极易溶于水,密度比空气小,所以可以采用向下排空气法收集,应选用的收集装置是D。
CaCl2+NH3+H2O;氨气极易溶于水,密度比空气小,所以可以采用向下排空气法收集,应选用的收集装置是D。

【题目】学习热情和学习方法是成才的必备条件,灵活掌握不同的学习方法可以取得事半功倍的效果.请用以下方法解决下列问题:
![]() 分类法:利用下列
分类法:利用下列![]() 组物质
组物质
![]() .
.![]() 、
、![]() 、
、![]() 、
、![]()
![]() .
.![]() 、
、![]() 、
、![]() 、
、![]()
![]() .金刚石与石墨的混合物、过氧化氢的水溶液、冰与水混合、氧气与臭氧混合
.金刚石与石墨的混合物、过氧化氢的水溶液、冰与水混合、氧气与臭氧混合
请按要求填写如表空白(填写物质的化学式或分类标准)
序号 |
|
|
|
分类标准 | 金属氧化物 | ________ | ________ |
属于该类别的物质 | ________ |
| ________ |
![]() 对比法:
对比法:
![]() .如图
.如图![]() 所示:其实验目的是探究________.
所示:其实验目的是探究________.
![]() .如图
.如图![]() 所示:杰克同学将盛有干燥白磷的甲试管和干燥红磷的乙试管插入盛有
所示:杰克同学将盛有干燥白磷的甲试管和干燥红磷的乙试管插入盛有![]() 的烧杯里(甲、乙试管均套有气球密封).过一会后,发现甲试管中的白磷燃烧,乙试管中的红磷没有燃烧.请根据杰克同学的实验现象,对比得出可燃物燃烧所需的条件之一:________.
的烧杯里(甲、乙试管均套有气球密封).过一会后,发现甲试管中的白磷燃烧,乙试管中的红磷没有燃烧.请根据杰克同学的实验现象,对比得出可燃物燃烧所需的条件之一:________.
【题目】某校化学兴趣小组的同学在老师的指导下做了有关氧气系列探究实验:
探究一:学习了二氧化锰对过氧化氢分解有催化作用的知识后,某同学想:CuO(氧化铜)能否起到类似二氧化锰的催化作用呢?于是进行了以下探究。
(猜想)Ⅰ.CuO不是过氧化氢分解反应的催化剂 Ⅱ.CuO是过氧化氢分解反应的催化剂。
(实验)用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如下实验:
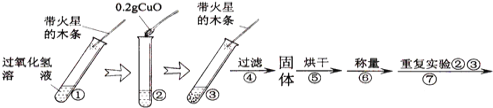
(1)
步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
__________ | __________ | 溶液中有气泡放出,______ | 猜想Ⅰ不成立; 猜想Ⅱ成立. |
(2)能证明CuO加快了过氧化氢分解速率的实验步骤是_________________。
(3)步骤⑦的目的是________________________。
探究二:对空气中氧气含量的测定实验进行探究:
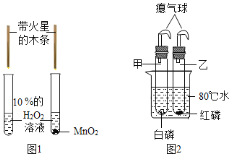
某化学兴趣小组对教材中“测定空气里氧气含量”的实验(见图Ⅰ)进行了大胆改进,设计(如图 Ⅱ)(选用容积为40mL试管作反应容器)实验方案进行,收到了良好的效果。请你对比分 析下面图Ⅰ、图Ⅱ实验,回答下列有关问题:
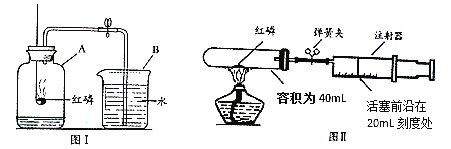
(1)图Ⅰ实验中:红磷在空气中燃烧(如图);该反应的文字表达式___;
(2)图Ⅱ实验中:
①实验前,打开弹簧夹,将注射器活塞前沿从20mL刻度处推至15mL刻度处,然后松开手,若活塞仍能返回至20mL刻度处,则说明___________________;
②图Ⅱ实验,若打开弹簧夹,用酒精灯加热红磷,从红磷燃烧到熄灭冷却的实验过程中,注射器活塞将___________________移动,最终约停止在____mL刻度处。
(3)反思:小林同学利用图Ⅰ装置测定空气中氧气的含量,若整个实验过程中忘记夹弹簧夹, 则最终液面上升的高度约 ____瓶内空气体积的 ![]() 。(填“大于”或“小于”)
。(填“大于”或“小于”)