题目内容
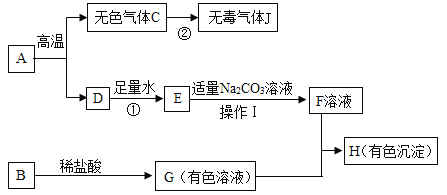
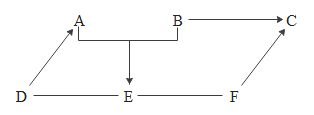
【题目】A、B、C、D、E是初中化学中常见的物质,其中E是六大基本营养素之一。它们之间转化关系如图所示:
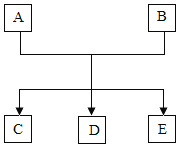
(1)若A是酸,C是食盐的主要成分,反应的化学方程式为__________。
(2)若在加热条件下,单质A能与B的浓溶液发生反应,且C溶液为蓝色,D会形成酸雨,D中组成元素的质量比为1∶1,则D的化学式为________。
(3)若A是碱,D是具有刺激性气味的气体,反应的化学方程式为_______。
【答案】![]() 或
或![]() SO2
SO2 ![]()
【解析】
(1)若A是酸,C是食盐的主要成分,则C是氯化钠,A能与B反应生成C、D、E,则A是盐酸,B是碳酸钠或碳酸氢钠,E是六大基本营养素之一,E是水,反应是碳酸钠和盐酸生成氯化钠、水和二氧化碳,或碳酸氢钠和盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式为:![]() 或
或![]() 。
。
(2)若在加热条件下,单质A能与B的浓溶液发生反应,且C溶液为蓝色,C是硫酸铜,D会形成酸雨,D中组成元素的质量比为1∶1,D是二氧化硫,则D的化学式为SO2。
(3)若A是碱,D是具有刺激性气味的气体,可推出D是氨气,E是六大基本营养素之一,E是水,A可以是氢氧化钙,B可以是氯化铵,反应是氢氧化钙和氯化铵生成氯化钙、水和氨气,反应的化学方程式为![]() 。
。

 阅读快车系列答案
阅读快车系列答案【题目】下列是关于 CO2 的实验室制法及性质实验,
|
|
|
|
A制 CO2 的药品 | B发生装置 | C收集装置 | D比较 CO2 与空气的密度 |
(1)其中有一项是不正确的,错误之处在于______________。
(2)D实验可以得出二氧化碳的化学性质是_______________,依据的现象是____________。解释该现象产生的原因_______________。
【题目】某校化学兴趣小组欲探究 CO2 与 NaOH 溶液反应后的溶质组成。
(查阅资料)20℃时,几种物质在水中的溶解度(S):
物质 | Na2CO3 | NaHCO3 | Ca(OH)2 | Ba(OH)2 | NaOH |
S/g | 21.5 | 9.6 | 0.165 | 3.89 | 109 |
(实验探究Ⅰ)
实验一:取两只充满 CO2 的矿泉水瓶,分别加入50mL 的水和等体积的 NaOH 溶液,立即拧紧瓶盖, 实验如图,充分振荡。瓶子变瘪程度 A______B(填 “>”“=”“<”)。
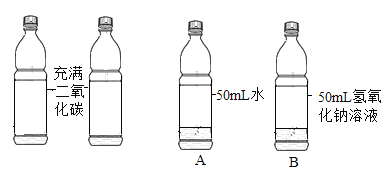
实验二:验证 B 瓶中反应生成了 Na2CO3:取少量 B 瓶中的溶液,滴加过量 BaCl2 的溶液,有白色沉淀生成,静置。
(1)该反应的化学方程式为______。
(2)实验中不宜将 BaCl2 溶液换成 CaCl2 溶液,原因是______。
实验三:取少量实验二中的上层清液,滴入几滴酚酞。
(3)溶液变红色。说明清液中还有 NaOH。
(4)实验二中必须加入过量的 BaCl2 溶液,理由是______。
(实验探究Ⅱ)
(查阅资料)
(1)本实验条件下,NaOH 溶液、Na2CO3 溶液和NaHCO3 溶液的 pH 分别约为 14.0、12.0和 8.5。
(2)将 CO2 通入少量的澄清石灰水中,溶液变浑浊,继续通 CO2 气体,浑浊逐渐消失, 其消失过程中发生的反应为:CaCO3 + H2O + CO2 =Ca(HCO3)2
(提出猜想)过量 CO2 与 NaOH 溶液反应后的溶质中还可能含有______(填化学式)。
(进行实验)小明在老师的帮助下利用数字传感器完成了以下实验。室温(约 20℃)下, 将 8gNaOH 溶于 190g 水中,然后向其中持续通入二氧化碳气体,同时用数字传感器测定溶液的 pH 变化,所得数据如图 2 所示。
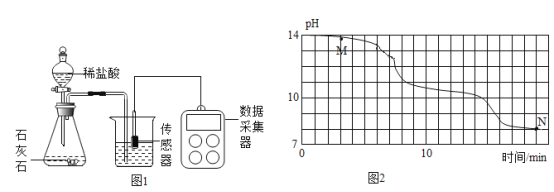
(得出结论)
(1)实验中,用“分液漏斗”而不用“长颈漏斗”的原因是______;
(2)根据资料和图像判断:M点溶质应为______(填化学式);
(反思交流)
(1)经多次重复实验,所得实验结果基本一致。实验过程中发现 18min 后溶液的 pH 基本不再变化,则此时烧杯内______(填“有”或“无”)晶体析出,原因是______。
(2)待 pH 不再变化后,取适量溶液,向其中滴加几滴稀盐酸,立即产生气泡,该反应的化学方程式为_______。
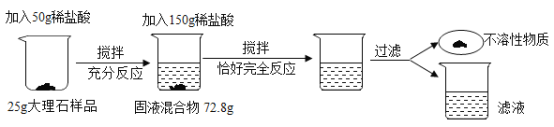
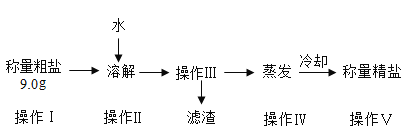
【题目】某小组同学欲提纯粗盐(只含氯化钠和少量泥沙)样品,实验过程和氯化钠的溶解度数据如下。
温度(°C) | 10 | 20 | 30 | 40 | 60 |
溶解度/g/100g水 | 35.8 | 36.0 | 36.1 | 36.4 | 37.1 |
(1)30°C时氯化钠的溶解度是______________。
(2)操作Ⅲ的名称是______________,其原理是依据_____________的性质进行提纯。
(3)最终提纯所得精盐质量偏少,可能的原因是______________ (选填编号)。
a 操作II中食盐未完全溶解就进行操作Ⅲ
b 操作Ⅲ中有滤渣漏入承接液体的烧杯
c 操作II、IV实验过程中有物质溅出
d 操作IV蒸发最终所得精盐比较潮湿
(4)溶解粗盐时,加入20°C水合适的量约为_____________(选填“20”、“30” 或“50”) mL。
(5)称取4.5g提纯的精盐,可配制质量分数为0.9%的食盐溶液______________g。