题目内容
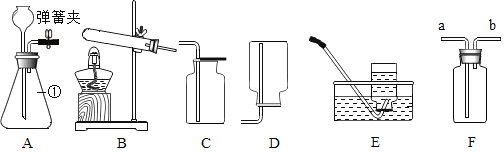
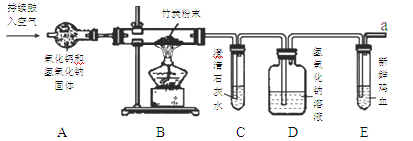
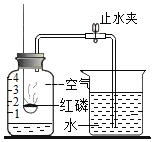
【题目】有一包白色固体样品,可能由硫酸钠、氢氧化钠、碳酸钙、氯化钡、氯化镁中的一种或几种物质组成,为探究该样品的组成,某小组取适量样品按下列流程进行试验。

请回答下列问题:
(查阅资料)CO2不能直接与BaCl2和MgCl2发生反应。
(1)过滤操作中用到的玻璃仪器有烧杯、漏斗、______。
(2)滤渣a的成分是______;白色沉淀b的成分是______。
(3)滤渣a中加入足量稀盐酸的目的:______。
(4)若现象①“滤渣全部溶解”变为“滤渣部分溶解”,其他现象不变,则原样品一定存在的物质是_____。
【答案】玻璃棒 CaCO3、Mg(OH)2(填名称也可) BaCO3(填名称也可) 排除硫酸钡沉淀的干扰,证明样品中无硫酸钠 CaCO3、BaCl2、Na2SO4、NaOH(填名称也可)
【解析】
碳酸钙难溶于水,钡离子和硫酸根离子会生成硫酸钡沉淀,氢氧化钠和氯化镁反应会产生氢氧化镁沉淀,碳酸钙和盐酸反应会生成二氧化碳气体,样品加水溶解,得到1.5g的滤渣,滤渣中加入足量的稀盐酸,完全溶解,有气泡产生,所以样品中一定含有碳酸钙,硫酸钠和氯化钡只能含有一种,滤液中通入二氧化碳,有白色沉淀生成,所以样品中一定含有氢氧化钠、氯化钡;
(1)过滤操所用到的玻璃仪器有烧杯、漏斗、玻璃棒;
(2)样品溶于水得到滤渣1.5g,能够全部溶于稀盐酸,且产生0.44g的二氧化碳,说明沉淀一定含有碳酸钙,一定没有硫酸钡;
设产生0.44g的二氧化碳需要碳酸钙的质量为x:
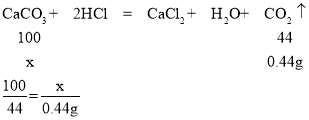
x=1g<1.5g,因此沉淀还有氢氧化镁,所以滤渣中含有原混合物中的CaCO3和反应生成的Mg(OH)2;
由分析可知,白色沉淀b的成分是BaCO3;
(3)滤渣a中加入足量稀盐酸的目的排除硫酸钡沉淀的干扰,证明样品中无硫酸钠;
(4)“滤渣部分溶解”,其他现象不变,则原样品一定存在的物质是CaCO3、BaCl2、Na2SO4、NaOH。

【题目】(1)如图一为某化学反应的微观示意图,其中不同的圆球代表不同的原子。关于该反应,下列说法正确的是_____。
A 反应前后分子的种类发生了改变
B 参加反应的两种分子个数比为3:2
C 反应后分子个数变少了
D 反应前后原子的数目没有增减
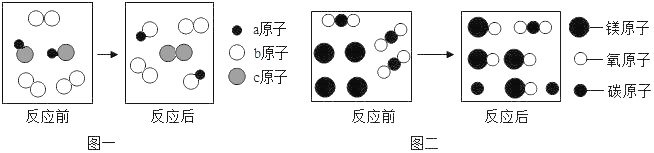
(2)图二是镁在点燃条件下与某物质发生化学反应的微观示意图,其中“●”表示碳原子,“〇”表示氧原子,“●”表示镁原子,该反应的化学方程式为_____。
(3)如表为处理汽车尾气化学反应微观示意图,其中A、B.、C、D表示4种物质,A和B在一定条件下反应可生成C和D.
反应前 | 反应后 |
| ||
A | B | C | D | |
|
|
|
| |
根据上述微观示意图,处理汽车尾气后的C和D质量比为_____。
【题目】向下表中的乙物质中逐渐加入一定质量的甲物质至过量,其相关量y与所加乙物质的质量关系与如图不相符的是( )
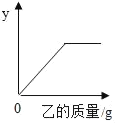
选项 | 甲 | 乙 | y |
A | Zn | 稀硫酸 | 生成气体的质量 |
B | NaOH溶液 | FeCl3溶液 | 混合后溶液的质量 |
C | Al2O3 | 稀盐酸 | 生成水的质量 |
D | CaCl2溶液 | Na2CO3 | 生成沉淀的质量 |
A. AB. BC. CD. D
【题目】我国自主设计的大型客机成功试飞,首艘国产航母正式下水,标志着我国的金属材料制造技术取得重大突破。根据所学知识回答下列问题:
(1)常温下一些金属的物理性质数据如表。据此可知高压输电线最好选用金属______;(填字母);C 的合金通常可以做菜刀、锤子等,其合金的硬度______5 (填“>”、“<”或“=”)
金属 | A | B | C | D |
导电性(以100为标准) | 99 | 61 | 17 | 7.9 |
密度/(g·cm2) | 8.92 | 2.70 | 7.86 | 11.3 |
熔点/℃ | 1083 | 660 | 1535 | 327 |
硬度(以10为标准) | 3 | 2.7 | 5 | 1.5 |
(2)铁矿石有多种,如赤铁矿(主要成分 Fe2O3)和磁铁矿(主要成分 Fe3O4)等。写出磁铁矿的主要成分与一氧化碳反应的化学方程式 ______。
(3)在Fe(NO3)2 和 AgNO3 的混合溶液中,加入一定量镁粉和锌粉的混合物,充分反应后过滤,得到滤渣和滤液。下列说法中正确的是______ (填序号)。
a.若滤液为浅绿色,则滤渣中可能有锌
b.滤液中一定有 Mg(NO3)2,滤渣中一定有银
c.若取少量滤液,加入 KCl溶液,无明显现象,则滤渣中一定有铁
d.若取少量滤渣,加入稀盐酸,产生气泡,则滤渣的组成有三种情况