题目内容
【题目】某兴趣小組为测定石灰石中碳酸钙的质量分数,取12g石灰石样品加入烧杯中,将120g稀盐酸平均分四次加入,充分反应后(杂质不溶于水也不与稀盐酸反应),测得实验数据如下:
实验次数 | 第一次 | 第二次 | 第三次 | 第四次 |
加入稀盐酸的质量/g | 30 | 30 | 30 | 30 |
剩余固体的质量/g | 9 | 6 | 3 | 2 |
分析数据计算(結果精确到0.1%):
(1)该祥品中碳酸钙的质量分数为__________。
(2)所用稀盐酸的溶质质量分数为__________。
(3)12g样品中的碳酸钙恰好完全反应时所得溶液的溶质质量分数为__________。
【答案】 83.3% 7.3% 10.5%
【解析】(1)由图可知,最终剩余固体的质量为2g,故混合物中碳酸钙的质量为12g-2g=10g,故样品中碳酸钙的质量分数为![]() ×100%=83.3% ;
×100%=83.3% ;
(2)以第一次的使用数据为准,每30g的稀盐酸可以反应3g的碳酸钙,设30g稀盐酸中溶质的质量为x
CaCO3+2HCl == CaCl2+H2O+CO2↑
100 73
3 x
![]() =
=![]() ,解得x=2.19g,故稀盐酸的质量分数为2.19g÷30g×100%=7.3%
,解得x=2.19g,故稀盐酸的质量分数为2.19g÷30g×100%=7.3%
(3)12g 的样品中碳酸钙的质量为10g,设10g的碳酸钙完全反应生成氯化钙的质量为y,生成二氧化碳的质量为m
CaCO3+2HCl == CaCl2+H2O+CO2↑
100 111 44
10g y m
![]() =
=![]() =
=![]() ,解得y=11.1g,m=4.4g;
,解得y=11.1g,m=4.4g;
由上可知,每3g的碳酸钙与30g 的稀盐酸完全反应,故10g的碳酸钙完全反应需要稀盐酸的质量为100g,故反应后溶液的总质量为10g+100g-4.4g=105.6g
故反应后溶液中溶质的质量分数为![]() ×100%=10.5%
×100%=10.5%

【题目】为探究CO2与NaOH溶液发生的反应,某兴趣小组尝试用不同的方式进行实验。
(查阅资料)
Ⅰ.20℃时,几种物质在水中的溶解度见下表:
物质 | Na2CO3 | NaHCO3 | Ca(OH)2 | Ba(OH)2 |
溶解度/g | 21.5 | 9.6 | 0.165 | 3.89 |
Ⅱ.本实验条件下,Na2CO3溶液和NaHCO3溶液的pH分别约为11.0和8.5。
(实验探究)
(1)实验一:小雨取一充满CO2的矿泉水瓶,加入一定量的水,立即拧紧瓶盖,振荡,发现瓶子变瘪,小雨另取一相同的充满CO2的矿泉水瓶,向其中加入与水等体积的NaOH溶液,立即拧紧瓶盖,振荡,得到溶液X,此时观察到的现象是_________________________________,实验中,小雨采用两只矿泉水瓶做对比实验的目的是_________________________________。
(2)实验二:为检验CO2与NaOH溶液反应的产物,小亮取实验一所得溶液X少许,向其中滴加BaCl2溶液,有白色沉淀产生,该反应的化学方程式为_____________________________,实验中不宜将BaCl2溶液换成CaCl2溶液的原因是_____________________________________。
(3)实验三:小华取实验一所得溶液X少许,向其中加入过量的BaCl2溶液,振荡,静置,取上层清液,滴入1滴酚酞试液,发现溶液呈____色,证明溶液X中有NaOH剩余。实验中,小华没有直接向少量溶液X中滴入酚酞试液,理由是___________________________________。
(4)实验四:兴趣小组将CO2持续通入一定浓度一定量的NaOH溶液中,用数字化实验技术测定反应过程中溶液的pH和温度变化,结果如图1、图2所示。
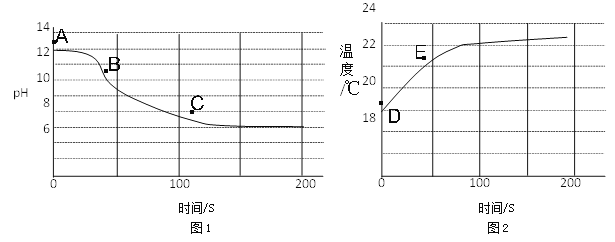
图1中,BC段发生反应的化学方程式为____________________________________。
图2中,DE段温度变化的原因是__________________________________________。
(反思感悟)
(5)实验从CO2减少、NaOH减少,Na2CO3生成等物质的变化,以及___________转化等视角多维度探究CO2与NaOH发生了反应,对于现象不明显的化学反应,可以通过现代技术手段进行数据测定,实现反应过程的“可视化”。
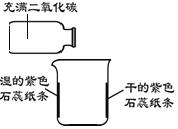
【题目】实验小组同学通过以下实验研究二氧化碳的性质。
| ①在烧杯内壁上贴上干的和用水润湿的紫色石蕊纸条 ②将充满二氧化碳的集气瓶轻轻在烧杯上方倾斜 | 一段时间后,湿的紫色石蕊纸条变为红色 |
(1)烧杯内壁上贴干的紫色石蕊纸条的目的是__________。
(2)该实验发生反应的化学方程式为__________。
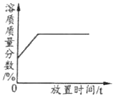
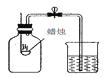
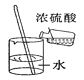
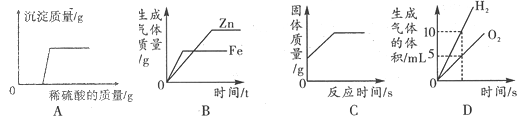
【题目】下表中,有关量的变化图像与其对应叙述相符的是
A | B | C | D |
|
|
|
|
浓硫酸敞口放置一段时间 | 向一定质量的氧化铁粉末中加入稀盐酸 | 向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn粉 | 向一定质量的二氧化锰中加入过氧化氢溶液 |
A. A B. B C. C D. D
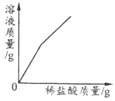
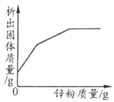
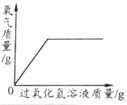
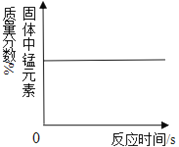
【题目】下列图像中,能体现对应变化关系趋势的是( )
|
|
|
|
A.一定质量的铁与足量的硫酸铜溶液反应 | B.镁在空气中点燃 | C.加热一定质量的氯酸钾和二氧化锰混合物 | D.向一定质量的二氧化锰中加入过氧化氢溶液 |
A. A B. B C. C D. D