题目内容
某同学利用日常生活中常见的用品制作了一套如图装置,用该装置对粗锌样品进行实验.请帮助完成下列实验报告(1)实验目的:测定______.
(2)实验用品:托盘天平、药水瓶、铜网、铜丝、饮料瓶、粗锌、稀盐酸、碱石灰(CaO与Na0H的混合物).
(3)实验步骤:
| 实验内容和步骤 | 实验现象 | 结论(或化学方程式) |
| ①称量10.0g粗锌放在铜网中,按图示装置组装后,称得仪器和药品总质量为120.0g | ||
| ②将铜网插入足量稀盐酸中,充分反应 | 发生的化学方程式: | |
| ③反应完全后,称得装置总质量为119.8g | 产生H2的质量为______g. 粗锌的纯度为______ |
①该实验中碱石灰的作用是______,若去掉碱石灰,则所测定的粗锌纯度______(填“偏大”、“偏小”、“无影响”).
②若只将粗锌换成石灰石,原实验方案能否用于石灰石样品纯度的测定______(填“能”或“不能”),理由是______.
③若将图中药水瓶改成直导管、粗锌换成纯锌,用原方案测定锌的相对原子质量,则结果______.(填“偏大”、“偏小”、“无影响”)

【答案】分析:(1)根据题目信息和实验步骤的数据可知实验目的.
(3)锌和盐酸反应生成氯化锌和氢气;质量的变化值就是氢气的质量,然后可以算出锌的质量.
(4)①氢气的质量是前后的质量的变化值,所以一定要防止其他物质出去,盐酸具有挥发性,碱石灰可以和盐酸反应,这样变化值就不会改变.没有碱石灰,氯化氢气体就会出去,导致质量的变化值增大,算出的锌的质量也会增大.
②碳酸钙和盐酸生成二氧化碳,二氧化碳会被碱石灰吸收,所以质量的变化值为零.
③没有碱石灰,氯化氢气体就会出去,导致质量的变化值增大,算出的锌的相对原子质量就会偏小.
解答:解:(1)根据题目信息和步骤数据,我们可以算出氢气和锌的质量,故答案为:粗锌的纯度.
(3)②锌和盐酸反应生成氯化锌和氢气,注意化学方程式的配平和气体符号,故答案为:Zn+2HC1=ZnC12+H2↑
③根据化学反应,反应前后只有氢气可以出去,因此质量的变化值是氢气的质量,即氢气的质量=120-119.8=0.2克.
设生成0.2克氢气需要锌的质量是X.
Zn+2HC1=ZnC12+H2↑
65 2
X 0.2克
 ═
═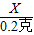 ,得:X=6.5克
,得:X=6.5克
∴粗锌的纯度= ×100%═65%.
×100%═65%.
故答案为:0.2,65%.
(4)①氢气的质量是前后的质量的变化值,所以一定要防止其他物质出去,盐酸具有挥发性,碱石灰可以和盐酸反应,这样变化值就不会改变.没有碱石灰,氯化氢气体就会出去,导致质量的变化值增大,算出的锌的质量也会增大.故答案为:防止饮料瓶中水蒸气和HCl气体随H2逸出,偏大.
②碳酸钙和盐酸生成二氧化碳,二氧化碳会被碱石灰吸收,所以质量的变化值为零.故答案为:不能,CO2会被碱石灰吸收不能逸出.
③没有碱石灰,氯化氢气体就会出去,导致质量的变化值增大,即氢气的质量就变大,设氢气的质量是X,锌的相对原子质量是Y.
Zn+2HC1=ZnC12+H2↑
Y 2
10克 X
 ═
═ ,得:Y=
,得:Y=
从表达式可以看出,X(氢气的质量)越大,则Y(锌的相对原子质量)就越小,故答案为:偏小.
点评:首先知道质量的变化值就是氢气的质量,然后写出化学方程式计算即可,学会判断“偏大”和“偏小”的分析方法.
(3)锌和盐酸反应生成氯化锌和氢气;质量的变化值就是氢气的质量,然后可以算出锌的质量.
(4)①氢气的质量是前后的质量的变化值,所以一定要防止其他物质出去,盐酸具有挥发性,碱石灰可以和盐酸反应,这样变化值就不会改变.没有碱石灰,氯化氢气体就会出去,导致质量的变化值增大,算出的锌的质量也会增大.
②碳酸钙和盐酸生成二氧化碳,二氧化碳会被碱石灰吸收,所以质量的变化值为零.
③没有碱石灰,氯化氢气体就会出去,导致质量的变化值增大,算出的锌的相对原子质量就会偏小.
解答:解:(1)根据题目信息和步骤数据,我们可以算出氢气和锌的质量,故答案为:粗锌的纯度.
(3)②锌和盐酸反应生成氯化锌和氢气,注意化学方程式的配平和气体符号,故答案为:Zn+2HC1=ZnC12+H2↑
③根据化学反应,反应前后只有氢气可以出去,因此质量的变化值是氢气的质量,即氢气的质量=120-119.8=0.2克.
设生成0.2克氢气需要锌的质量是X.
Zn+2HC1=ZnC12+H2↑
65 2
X 0.2克
 ═
═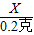 ,得:X=6.5克
,得:X=6.5克∴粗锌的纯度=
 ×100%═65%.
×100%═65%.故答案为:0.2,65%.
(4)①氢气的质量是前后的质量的变化值,所以一定要防止其他物质出去,盐酸具有挥发性,碱石灰可以和盐酸反应,这样变化值就不会改变.没有碱石灰,氯化氢气体就会出去,导致质量的变化值增大,算出的锌的质量也会增大.故答案为:防止饮料瓶中水蒸气和HCl气体随H2逸出,偏大.
②碳酸钙和盐酸生成二氧化碳,二氧化碳会被碱石灰吸收,所以质量的变化值为零.故答案为:不能,CO2会被碱石灰吸收不能逸出.
③没有碱石灰,氯化氢气体就会出去,导致质量的变化值增大,即氢气的质量就变大,设氢气的质量是X,锌的相对原子质量是Y.
Zn+2HC1=ZnC12+H2↑
Y 2
10克 X
 ═
═ ,得:Y=
,得:Y=
从表达式可以看出,X(氢气的质量)越大,则Y(锌的相对原子质量)就越小,故答案为:偏小.
点评:首先知道质量的变化值就是氢气的质量,然后写出化学方程式计算即可,学会判断“偏大”和“偏小”的分析方法.

练习册系列答案
相关题目
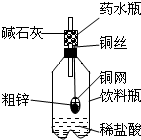 某同学利用日常生活中常见的用品制作了一套如图装置,用该装置对粗锌样品进行实验.请帮助完成下列实验报告
某同学利用日常生活中常见的用品制作了一套如图装置,用该装置对粗锌样品进行实验.请帮助完成下列实验报告(1)实验目的:测定
(2)实验用品:托盘天平、药水瓶、铜网、铜丝、饮料瓶、粗锌、稀盐酸、碱石灰(CaO与Na0H的混合物).
(3)实验步骤:
| 实验内容和步骤 | 实验现象 | 结论(或化学方程式) |
| ①称量10.0g粗锌放在铜网中,按图示装置组装后,称得仪器和药品总质量为120.0g | ||
| ②将铜网插入足量稀盐酸中,充分反应 | 发生的化学方程式: | |
| ③反应完全后,称得装置总质量为119.8g | 产生H2的质量为 粗锌的纯度为 |
①该实验中碱石灰的作用是
②若只将粗锌换成石灰石,原实验方案能否用于石灰石样品纯度的测定
③若将图中药水瓶改成直导管、粗锌换成纯锌,用原方案测定锌的相对原子质量,则结果
 某同学利用日常生活中常见的用品制作了一套如图装置,用该装置对粗锌样品进行实验.请帮助完成下列实验报告
某同学利用日常生活中常见的用品制作了一套如图装置,用该装置对粗锌样品进行实验.请帮助完成下列实验报告
(1)实验目的:测定______.
(2)实验用品:托盘天平、药水瓶、铜网、铜丝、饮料瓶、粗锌、稀盐酸、碱石灰(CaO与Na0H的混合物).
(3)实验步骤:
| 实验内容和步骤 | 实验现象 | 结论(或化学方程式) |
| ①称量10.0g粗锌放在铜网中,按图示装置组装后,称得仪器和药品总质量为120.0g | ||
| ②将铜网插入足量稀盐酸中,充分反应 | 发生的化学方程式: | |
| ③反应完全后,称得装置总质量为119.8g | 产生H2的质量为______g. 粗锌的纯度为______ |
①该实验中碱石灰的作用是______,若去掉碱石灰,则所测定的粗锌纯度______(填“偏大”、“偏小”、“无影响”).
②若只将粗锌换成石灰石,原实验方案能否用于石灰石样品纯度的测定______(填“能”或“不能”),理由是______.
③若将图中药水瓶改成直导管、粗锌换成纯锌,用原方案测定锌的相对原子质量,则结果______.(填“偏大”、“偏小”、“无影响”)
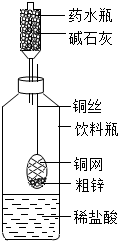 某同学利用日常生活中常见的用品制作了一套如图装置,用该装置对粗锌样品进行实验.请你帮助完成下列实验报告.
某同学利用日常生活中常见的用品制作了一套如图装置,用该装置对粗锌样品进行实验.请你帮助完成下列实验报告. 某同学利用日常生活中常见的用品制作了一套如图装置,用该装置对粗锌样品进行实验.请帮助完成下列实验报告.
某同学利用日常生活中常见的用品制作了一套如图装置,用该装置对粗锌样品进行实验.请帮助完成下列实验报告. 某同学利用日常生活中常见的用品制作了一套如图装置,用该装置对粗锌样品进行实验.请你帮助完成下列实验报告.
某同学利用日常生活中常见的用品制作了一套如图装置,用该装置对粗锌样品进行实验.请你帮助完成下列实验报告.