题目内容
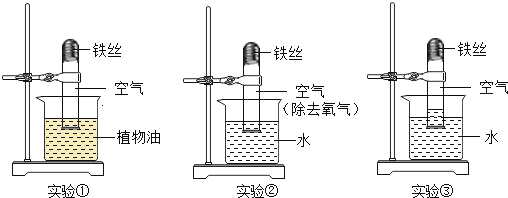
【题目】某校化学兴趣小组进行了甲、乙两个实验。
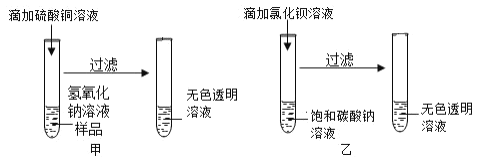
(1)甲实验中反应的化学方程式为_____;
(2)乙实验观察到的现象是_____。
(3)实验结束后,小组同学把实验后的两支试管的溶液倒入同一个烧杯中,发现烧杯中仅得到无色溶液,他们决定对烧杯中溶液的溶质成分进行探究。
(提出问题)烧杯中溶液的溶质成分是什么?
一致认为认为溶液的溶质一定有Na2SO4和_____;溶质中还可能有什么?
(进行猜想)小明认为烧杯中溶液的溶质可能有NaOH,小亮认为烧杯中溶液的溶质可能有_____;小红认为烧杯中溶液的溶质可能有Na2CO3和NaOH。
(验证猜想)
实验操作 | 现象 | 结论 |
①取少量烧杯中的溶液于试管,测定pH. | pH>7 | 溶液呈_____性 |
②另取少量烧杯中的溶液于试管中,滴加足量BaCl2溶液,静置,再滴加无色酚酞。 | _____, 溶液由无色变为红色。 | 小红的猜想成立 |
(结论分析)小刚认为实验操作②的结论不严谨,因为_____(用文字表述);若要确定小红的猜想是否成立,应另取少量烧杯中的溶液于试管中,滴加_____,然后观察是否有_____出现,反应的方程式为_____。
(拓展与思考)如果实验操作①中测得的pH=7,烧杯中溶液的溶质成分是_____;
可见,探究反应后所得物质的成分时,既要考虑生成物,还要考虑反应物是否过量。
(综合计算)向50g硫酸铜溶液中,逐滴加入NaOH溶液,加入NaOH溶液的质量与生成沉淀的质量之间的关系如图所示,请回答下列问题:
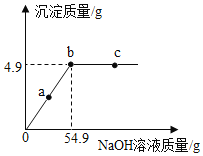
(1)恰好完全反应时,溶液的质量为_____g。
(2)求原硫酸铜溶液中溶质的质量分数_____(写出计算过程)。
(3)在实验过程中,以下说法正确的是_____。
A 0至b段溶液中溶质质量逐渐增加
B a、b、c点对应的溶液中溶质均为一种
C 向c点对应的溶液中滴加酚酞溶液,溶液变红
D 整个过程中,溶液中氢元素的质量一直在增加
【答案】![]() 有白色沉淀生成
有白色沉淀生成 ![]()
![]() 碱 出现白色沉淀 加入的氯化钡和硫酸钠溶液也能产生白色沉淀 硝酸钡溶液 白色沉淀
碱 出现白色沉淀 加入的氯化钡和硫酸钠溶液也能产生白色沉淀 硝酸钡溶液 白色沉淀 ![]()
![]() 50 16% CD
50 16% CD
【解析】
氢氧化钠和硫酸铜生成氢氧化铜蓝色沉淀和硫酸钠,氯化钡和碳酸钠反应生成碳酸钡白色沉淀和氯化钠,氯化钡和硫酸钠反应生成硫酸钡和氯化钠。
(1)甲实验中反应是氢氧化钠和硫酸铜生成氢氧化铜蓝色沉淀和硫酸钠,化学方程式为![]() 。
。
(2)乙实验中发生的反应是氯化钡和碳酸钠反应生成碳酸钡白色沉淀,故可看到有白色沉淀生成。
[提出问题]一致认为认为溶液的溶质一定有![]() 和
和![]() 。
。
[进行猜想]小明认为烧杯中溶液的溶质可能有NaOH,小亮认为烧杯中溶液的溶质可能有![]() ;小红认为烧杯中溶液的溶质可能有Na2CO3和NaOH。
;小红认为烧杯中溶液的溶质可能有Na2CO3和NaOH。
[验证猜想]
实验操作 | 现象 | 结论 |
①取少量烧杯中的溶液于试管,测定pH. | pH>7 | 溶液呈碱性 |
②另取少量烧杯中的溶液于试管中,滴加足量BaCl2溶液,静置,再滴加无色酚酞。 | 出现白色沉淀, 溶液由无色变为红色。 | 小红的猜想成立 |
[结论分析]小刚认为实验操作②的结论不严谨,因为加入的氯化钡和硫酸钠溶液也能产生白色沉淀;若要确定小红的猜想是否成立,应另取少量烧杯中的溶液于试管中,滴加硝酸钡溶液,硫酸钠和硝酸钡反应生成硫酸钡和硝酸钠,故观察是否有白色沉淀出现,反应的方程式为![]() 。
。
[拓展与思考]如果实验操作①中测得的pH=7,烧杯中溶液的溶质成分是![]()
可见,探究反应后所得物质的成分时,既要考虑生成物,还要考虑反应物是否过量。
[综合计算](1)恰好完全反应时,溶液的质量为![]() 。
。
(2)设原硫酸铜溶液中溶质的质量分数x

![]()
![]()
硫酸铜溶液中溶质的质量分数为16%。
(3)A、由图可知,0至b段溶液中沉淀逐渐增加,溶质质量逐渐减少,故A不正确;
B、a点对应的溶质是硫酸铜和硫酸钠,b点对应的溶质是硫酸钠,c点对应的溶液中溶质是氢氧化钠和硫酸钠,故B不正确;
C、向c点对应的溶液中溶质是氢氧化钠和硫酸钠,滴加酚酞溶液,溶液变红,故C正确;
D、整个过程中,氢氧化钠中的氢元素转化为氢氧化铜沉淀中的氢元素,而溶剂水中的氢元素进入溶液,则溶液中氢元素的质量一直在增加,故D正确。故选CD。

【题目】某白色固体可能由BaC12、NaOH、Na2CO3、Na2SO4;中的一种或几种物质组成,某兴趣小组的同学为确定该白色固体的成分,进行了如下的实验探究,请你参与并回答相关问题。
I.初步探究:小金同学设计的实验过程及现象如图所示。
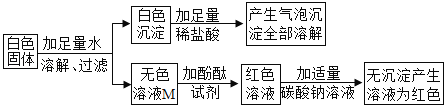
(查阅资料)BaC12溶液显中性。
(初步结沦)(1)原白色固体中一定有的物质是_____,一定没有的物质是_____。白色沉淀溶解的化学方程式是_____。
(2)M溶液中的溶质一定有_____,一定没有氯化钡。
(交流讨论)小英同学认为:无色溶液M变红色,说明溶液M中含有碱性物质,但不能由此推导出原固体物质中是否含有氢氧化钠。若要进一步确定,需对溶液M继续进行探究。为此同学们进行了如下的探究:
Ⅱ.继续探究:
(提出问题)无色溶液M中有氢氧化钠吗?
(猜想与假设)猜想一:有NaOH
猜想二:没有NaOH
(探究与结论)
实验步骤 | 实验现象 | 实验结论 |
A.取无色溶液M于试管中,加入过量的氯化钡溶液,振荡,静置 | _____ | 证明溶液M中有碳酸钠并被除尽 |
B.取实验A所得上层清液于试管中,加入_____。 | _____ | 猜想一正确 |
在老师的指导下,同学们通过交流、讨论、实验,圆满地完成了这次探究活动。