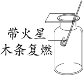题目内容
【题目】向盛有50g稀硫酸的小烧杯中,缓慢滴加氢氧化钡[Ba(OH)2]溶液至过量。发生中和反应为:H2SO4 + Ba(OH)2 = BaSO4↓+2H2O。烧杯中物质的某些量随着氢氧化钡溶液的滴加,其变化趋势中正确的是
A.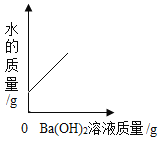 B.
B.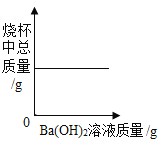 C.
C.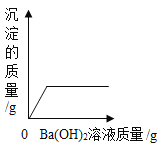 D.
D.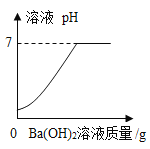
【答案】C
【解析】
A、不断慢慢滴加10%的Ba(OH)2溶液至恰好完全反应过程中除Ba(OH)2溶液中的水又与硫酸生成一部分水,再继续加入Ba(OH)2溶液,增加水的质量只是Ba(OH)2溶液中的水,因此两部分增加水的质量不一样多,故斜率不同,所以不正确;B、随着氢氧化钡溶液的加入,物质的总质量在不断增大,故错误;C、稀硫酸和氢氧化钡能反应生成硫酸钡沉淀和水,当硫酸反应完后,沉淀的质量不再改变,故正确;D、硫酸的pH小于7,当硫酸与氢氧化钡完全反应时溶液的pH等于7,加入氢氧化钡过量时,溶液的pH大于7,故错误。故选C。

 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
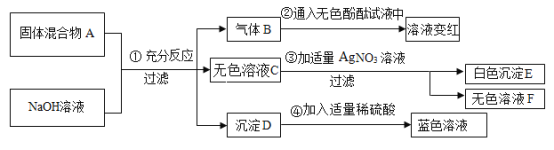
全能闯关100分系列答案【题目】某兴趣小组的同学发现放置在潮湿空气中的铁片和铜片均会被锈蚀。根据所学知识稀盐酸能除去铁锈,请写出该反应的化学方程式___________。同学们联想到能否用稀盐酸除去铜锈呢?于是他们取少量铜锈放在试管内滴加足量的稀盐酸发现铜锈溶解生成蓝色溶液的同时产生一种无色无味的气体这一现象引起大家的兴趣并进行了如下探究。
(提出问题)产生气体的成分是什么?
(作出猜想)结合空气中的气体成分及反应前后元素种类守恒同学们作出了如下猜想:
![]() 可能是氢气;
可能是氢气;![]() 可能是氧气;
可能是氧气;![]() 可能是二氧化碳;
可能是二氧化碳;
![]() 可能是氮气;
可能是氮气;![]() 可能是氨气。
可能是氨气。
(交流讨论)大家讨论后一致认为该气体肯定不是氨气理由是___________。
(进行实验)
实验操作及现象 | 实验分析 | |
(1) | 收集一试管产生的气体,将燃着的木条伸入试管内燃着的木条熄灭 | 说明该气体肯定不是 ___________ |
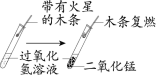
(2) | 再将产生的气体 ___________ | 说明该气体肯定不是氮气而是二氧化碳 |
(得出结论)稀盐酸除去铜锈时产生的无色无味的气体是![]() 。
。
(反思拓展)(1)根据上述实验过程你认为铜锈的成分是下列选项中的__________。
A铜盐 B铵盐 C碳酸盐 D氧化铜 E氢氧化铜
(2)根据铁生锈的条件类比推出:铜生锈是铜与空气中的__________共同作用的结果。
(3)铁片和铜片在外界条件相同时哪一种金属更易锈蚀__________?说明理由__________。