题目内容
2011年世界水日的主题是“城市用水:应对都市化挑战”。下图表示某市饮用
水的净化过程,请回答下列问题:
(1)地下水中的细菌和颗粒等杂质比湖水、河水等地表水中的少,请说出一个原因 。
(2)在图中“加絮凝剂”的目的是 ,常用的“絮凝剂”是 。
(3)如果自来水从配水泵传输到用户的过程中存在细菌污染,人们在家中饮用该水之前应该如何处理? 。
(4)野炊时,如果要初步过滤浑浊的河水用于煮饭,怎样用身边的物品(饮料瓶、手绢、细沙、小卵石等)制作一个简易净水器(图示或文字表示均可)。
(1)地下水经过了沙石、土壤等的过滤(或地表水易被污染等其他合理答案也可)
(2)吸附杂质,使杂质沉降 明矾
(3)加热煮沸(或加漂白粉等其他可在家中进行的合理方法也可)
(4)在切去底部、倒置的饮料瓶中,由下至上依次加入手绢、
细沙和小卵石(
解析试题分析:(1)地下水经过了沙石、土壤等的过滤,所以杂质比湖水、河水等地表水中的少;
(2)净化水的方法有沉淀、过滤、吸附、蒸馏。沉淀包括静止沉淀和吸附沉淀,吸附沉淀时水中要加明矾,作用是明矾溶于水形成胶状物吸附杂质,使杂质沉降,达到净水的目的;
(3)存在细菌要把它杀灭,可采用加热煮沸的方法;
(4)过滤可将固体和液体分离,但过滤只除去了难溶性物质,要用活性炭吸附水的颜色和异味,所以可以在切去底部、倒置的饮料瓶中,由下至上依次加入手绢、
细沙和小卵石、木炭等。
考点:水的净化

 阅读快车系列答案
阅读快车系列答案水是生命之源,它与我们的生活密切相关。
(1)净水中常用到明矾,它的作用是 ,生活中可用 区分软水和硬水。
(2)能确认水是由氧元素和氢元素组成的实验是 。
| A.氢气在氧气中燃烧只生成水 | B.水的蒸发 | C.水的电解 | D.水的净化 |
水是生命之源,通过化学学习,我们进一步认识到水的重要作用.
(1)请写出组成元素和水相同的物质的化学式 .
(2)自然界的水常常遭到人为污染.污染物中氮和磷含量过高会造成水中藻类过度繁殖,使水质恶化,这里的“氮和磷”是指 (填序号).
| A.元素 | B.原子 | C.离子 | D.分子 |
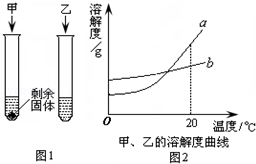
(4)20℃时,向两支试管中加入等质量的甲、乙两种固体物质,分别加入10g水,使其充分溶解,观察到如右图1所示的现象.20℃时, (填“甲”或“乙”)的溶液一定是饱和溶液.右图2中表示甲物质的溶解度曲线的是 (填“a”或“b”),将10℃a的饱和溶液升温到20℃,其溶质质量分数 (填“变大”、“变小”或“不变”).
某公司研制出了一种新颖的“装饰树”,下表为该产品介绍。
| 产品介绍 |
| “装饰树”表面涂了一层光触媒,这种光触媒是一种纳米级二氧化钛,能产生强烈的降解功能,能有效降解空气中的有毒有害气体,如甲醛、一氧化氮、二氧化硫、一氧化碳等。在降解过程中光触媒不挥发,不消耗,具有长效性。 |
(1)根据产品介绍可判断降解反应中二氧化钛是一种 (填“反应物”、“生成物”或“催化剂”)。
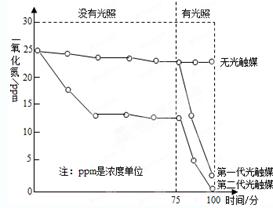
(2)上图是某科研小组探究两代光触媒降解一氧化氮的实验结果,由此可知:
①第一代光触媒产生强烈的降解作用的条件是 ;
②第二代光触媒与第一代光触媒相比,优点是 (写出一点即可)。