题目内容
【题目】某校研究性学习小组用下图所示装置进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶容积的70%. 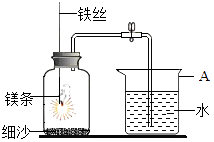
(1)图中镁条燃烧、冷却后打开止水夹,水能进入集气瓶中的原因是 .
(2)如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多不超过其容积的21%.现进入集气瓶中水的体积约为其容积的70%,根据空气的组成可推出减少的气体中有氮气.
【发现问题】氮气是怎么减少的呢?
【假设一】氮气与镁条反应而减少.
【假设二】 .
【查阅资料】镁条在氮气中能燃烧,产物为氮化镁(Mg3N2)固体,化学方程式为
N2+3Mg ![]() Mg3N2 . 镁条还可以在二氧化碳气体中燃烧生成碳和氧化镁.
Mg3N2 . 镁条还可以在二氧化碳气体中燃烧生成碳和氧化镁.
(3)通过以上探究,你对所学知识有了什么新的认识: .
【答案】
(1)集气瓶中镁与空气中的成分反应,压强减少,水能进入
(2)二氧化碳与镁条反应而减少
(3)燃烧不一定都需要氧气或镁着火不能用二氧化碳灭火等
【解析】解:(1)通过实验分析可知:图中镁条燃烧、冷却后打开止水夹,水能进入集气瓶中的原因是,集气瓶中镁与空气中的成分反应,压强减少,水能进入;所以答案是:集气瓶中镁与空气中的成分反应,压强减少,水能进入.

练习册系列答案
相关题目