题目内容
【题目】数字化实验设备含:传感器——数据采集器——计算机——应用软件,它可将实验过程中某些因素(酸碱性、浓度、气压等)的变化以数据、图像的形式呈现出来。
(查阅资料)
(1). 在0℃,标准大气压下,1体积水可以溶解1体积的二氧化碳。
(2). 酸碱度描述的是水溶液的酸碱性强弱程度,用pH值来表示。pH值越小,酸性越强,pH值越大,碱性越强。
(一)探究二氧化碳与水反应
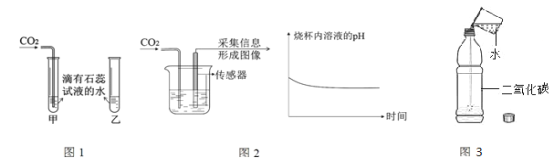
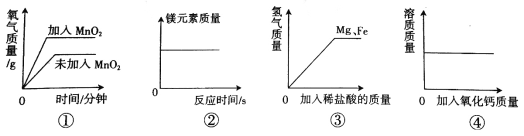
(1)图1中可观察到甲试管里的颜色变化_______________,该反应的符号表达式为______。你认为该同学验证CO2能与水反应的方法是通过证明_____
(填序号)。 A. 反应物被消耗 B.有新物质生成
其中乙试管的作用是_______________。
(2)由图2坐标图中的曲线可知,烧杯内溶液的酸性逐渐变_____(选填“强”或“弱”)。
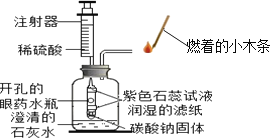
(3)某兴趣小组的同学采取图3装置探究CO2能与水反应。
①甲同学按如图3所示的实验,打开瓶塞,迅速将烧杯中的水倒入瓶中并拧紧瓶塞,振荡,一会后发现软塑料瓶变瘪。得出结论:CO2能与水反应。请你解释塑料瓶变瘪的原因是:___________。
②乙同学认为甲同学的实验,还不足以证明CO2能与水反应。乙同学的理由是: __________。
(二)探究蜡烛燃烧的产物
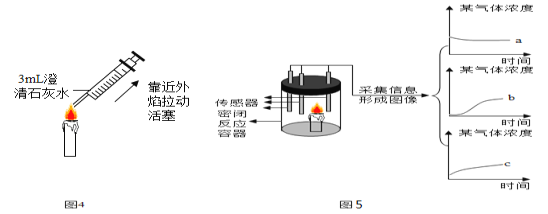
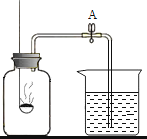
(4)如图4所示,用注射器在蜡烛外焰部位抽气并振荡,可观察到_______________,证明反应生成了二氧化碳。若将干冷的烧杯罩在火焰上方,观察到_______________,证明反应生成了水。
(5)如图5所示,蜡烛在密闭容器内燃烧,同时监测容器内氧气、二氧化碳和水蒸气含量的变化,形成三条曲线如坐标图所示,曲线________ (选填“a”、“b”、“c”)能够说明蜡烛燃烧生成了二氧化碳和水。
(三)比较块状碳酸钙、碳酸钙粉末与稀盐酸反应的速度
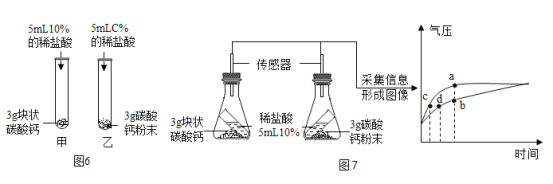
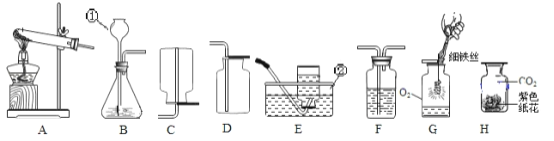
(6)写出碳酸钙与稀盐酸反应的符号表达式:___________________________。
(7)图6中,乙试管里稀盐酸的溶质质量分数C%应为________。较之块状碳酸钙,碳酸钙粉末与稀盐酸的反应更为剧烈,原因是___________________________。
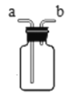
(8)按图7所示进行实验,倾斜锥形瓶使小试管内的稀盐酸流入瓶中与固体接触发生反应,瓶内气压的变化如坐标图所示。对比分析坐标图中的点________ (选填“a”、“b”、“c”、“d”) 可知:两个锥形瓶内达到相同的压强时,碳酸钙粉末与稀盐酸反应所需时间更短。
【答案】红CO2+H2O=H2CO3B对照实验强二氧化碳和水反应使塑料瓶中的压强小于外界压强,从而使塑料瓶变瘪。二氧化碳能够溶于水,也会使塑料中的压强减小。石灰水变浑浊,烧杯内壁有水雾。b、cCaCO3+2HCl→CaCl2+H2O+CO210%反应物之间的接触面积更大c、d.
【解析】
(1)甲试管中二氧化碳与水反应生成碳酸,故溶液变为红色。二氧化碳与水反应生成碳酸,反应的符号表达式为:CO2+H2O=H2CO3 。该实验中甲试管中有碳酸生成,乙试管中没有碳酸生成,而甲试管中变为红色,乙试管没有变红,故是通过有新物质生成来验证二氧化碳与水发生了反应,故选B。该实验中乙试管的作用是与甲试管进行对比。
(2)由坐标图可知,溶液的pH值减小,故酸性增强。
(3)①将水加入到装有二氧化碳气体的塑料瓶中后,二氧化碳能溶于水,且可以与水反应,故瓶内二氧化碳的含量减少,压强降低,故塑料瓶变瘪了。②二氧化碳能溶于水,且可以与水反应,故塑料瓶变瘪不能说明二氧化碳一定与水发生了反应,可能是由于二氧化碳溶于了水。
(4)蜡烛燃烧后生成了二氧化碳,被抽入装有澄清石灰水的针筒中后,澄清石灰水变浑浊。该实验的结论是有水生成,则在干燥的烧杯内有水雾出现。
(5)蜡烛燃烧的过程中氧气的含量减少,二氧化碳和水的含量增加,故曲线bc能够说明蜡烛燃烧生成了二氧化碳和水。
(6)碳酸钙与稀盐酸反应生成氯化钙、二氧化碳和水,反应的符号表达式为:CaCO3+2HCl→CaCl2+H2O+CO2。
(7)图6的实验目的是探究稀盐酸与碳酸钙的接触面积对反应速率的影响,故要求稀盐酸的浓度控制为一样,故稀盐酸的浓度为10%。粉末状的碳酸钙与稀盐酸的接触面积更大,故反应的速率更快。
(8)由图可知,cd两点瓶内的气压相同。

 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案【题目】兴趣小组的同学们在老师的指导下进行实验室制取氧气的实验。
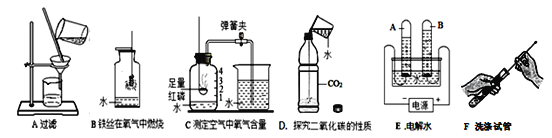
(1)甲同学称取一定质量的高锰酸钾固体放入大试管中,将温度控制在250℃加热制取O2。实验结束时,乙同学发现用排水法收集到的氧气大于理论产量。针对这一现象,进行了如下探究:
[提出猜想]猜想I:反应生成的二氧化锰分解放出氧气;猜想II:反应生成的锰酸钾分解放出氧气;猜想III:_________________
[实验验证]同学们分成两组,分别进行下列实验:第一组同学取一定质量的二氧化锰,在250℃条件下加热一段时间,冷却后测得二氧化锰的质量不变,则猜想______错误;第二组同学取锰酸钾在250℃条件下加热,没有用测定质量的方法得出了猜想II正确的结论。该组同学选择的实验方法是______________。
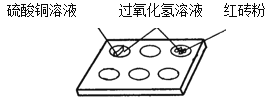
(2)白色点滴板是带有空穴的白色瓷板,可用作微型化学反应。在寻找新催化剂时,将一定量的红砖粉、硫酸铜溶液……分别加入点滴板中,再分别滴入过氧化氢溶液(如图所示),观察到过氧化氢溶液产生气泡的速率加快。据此现象得出结论:红砖粉、硫酸铜溶液等也能做过氧化氢溶液的催化剂。小红认为不正确,
理由一:未探究它们的质量在反应前后是否不变;
理由二:_______________________。
白色点滴板作为反应容器的优点有______________________
(3)通过对催化剂的实验探究,同学们还想探究影响反应速率的其他因素。于是在老师的指导下查阅资料,资料表明:影响反应速率的其他因素还有温度,浓度,物质的纯度和固体的形状大小等。根据查阅的资料同学们设计了实验室用锌与稀硫酸反应制取氢气的实验。反应过程中,用前 10 min 内收集的氢气体积比较反应的快慢。控制其他条件相同,进行下表四组实验,获得数据如下表。
验实号编 | 试剂 | 前 10 min 内产生的氢气体积(mL) | |
不同纯度的锌 | 不同体积和浓度的稀硫酸 | ||
a | 纯锌 | 30 mL 30 % | 564.3 |
b | 含杂质的锌 | 30 mL 30 % | 634.7 |
c | 纯锌 | 30 mL 20 % | 449.3 |
d | 纯锌 | 40 mL 30 % | 602.8 |
① 比较实验 a 和实验 b ,可以得到的结论是________________________。
② 为了研究硫酸浓度对反应快慢的影响,需比较实验_____和实验_____(填编号)。
③ 控制其他条件相同,需控制的条件是__________________(例举一种条件即可)。
通过实验,同学们明白了一个道理,物质的纯度对化学反应速率有很大影响,但是不一定是纯度越大反应速率越快,有时候也会有一些特殊情况。