题目内容
【题目】3g 某物质在 O2 中完全燃烧,生成 4.4gCO2 和 1.8gH2O。下列说法不正确的是
A.该物质的化学式可能是 C2H4O2
B.该物质中碳元素的质量分数为 40%
C.6g 该物质完全燃烧消耗 6.4g O2
D.3g 该物质在 2.4g O2 中燃烧,生成 3.3g CO2
【答案】D
【解析】
A、由质量守恒定律可知,参加反应的氧气质量为:4.4g+1.8g-3g=3.2g,该物质中碳元素质量为:4.4g×![]() =1.2g,氢元素质量为:1.8g×
=1.2g,氢元素质量为:1.8g×![]() =0.2g,氧元素质量为:4.4g-1.2g+1.8g-0.2g-3.2g=1.6g,该物质中碳原子、氢原子、氧原子个数比为:
=0.2g,氧元素质量为:4.4g-1.2g+1.8g-0.2g-3.2g=1.6g,该物质中碳原子、氢原子、氧原子个数比为:![]() :
:![]()
:![]() =1:2:1,因此该物质化学式可能是C2H4O2,该选项说法正确;
=1:2:1,因此该物质化学式可能是C2H4O2,该选项说法正确;
B、该物质中碳元素的质量分数为:![]() ×100%=40%,该选项说法正确;
×100%=40%,该选项说法正确;
C、3g该物质完全燃烧需要3.2g氧气,因此6g该物质完全燃烧消耗6.4gO2,该选项说法正确;
D、3g该物质完全燃烧需要3.2g氧气,3g该物质在2.4gO2中燃烧时,氧气不足,可能生成一氧化碳,因此生成二氧化碳质量不一定是3.3g,该选项说法不正确。
故选D。

 阅读快车系列答案
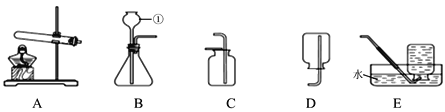
阅读快车系列答案【题目】化学反应速率是衡量化学反应进行快慢的物理量,为了探究影响化学反应速率的因素,以过氧化氢分解为研究对象进行实验。三个小组均可采用如图装置进行实验,记录收集 10mL 氧气的时间,实验室可供选择的试剂有:2.5%、5%、10%三种浓度的 H2O2 溶液、MnO2、CuO、红砖粉末。
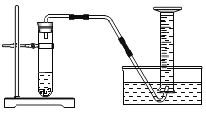
(A 组):探究催化剂对化学反应速率的影响
取 5mL10%H2O2 溶液,三次实验分别加入 0.5gMnO2、红砖粉末、CuO 进行实验,记录数据如下:
试剂 | MnO2 | 红砖粉末 | CuO |
t(秒) | 10 | 60 | 20 |
由此可出结论:MnO2、CuO 对 H2O2 分解有催化作用,红砖粉末无催化作用,某同学对该结论提出疑问。
补充对比实验,操作为__________。结果:长时间(大于 100s),收集到很少量气体。
更正结论:红砖粉末 _____(选填“有”、“无”)催化作用,三者中 _____催化效率最高。
(B 组):探究浓度对化学反应速率的影响
甲同学:取 10mL5%H2O2 溶液,加入 0.5gMnO2 为催化剂,进行实验,记录时间 t1。 乙同学:取 10mL2.5%H2O2 溶液,加入 0.5gMnO2 为催化剂,进行实验,记录时间 t2。 实验结果 _____。
结论:当催化剂种类相同时,反应物的浓度越大,反应速率越快。
(C 组):探究温度对化学反应速率的影响。
取 10mL5%H2O2 溶液和 0.5gCuO 为催化剂进行实验,两次实验分别将试管置于冰水浴和 50℃热水浴记录时间 t4、t5,且 t4>t5。
结论:当反应物浓度和催化剂相同时,____________。
综上所述:①为了研究某一因素对化学反应速率的影响,必须控制外界其他因素相同.
②探究发现影响化学反应速率的因素有____。