题目内容
【题目】结合下列图示的实验,回答有关问题:
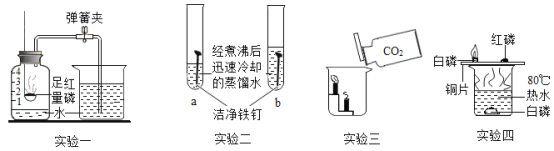
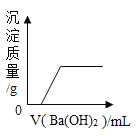
(1)实验一中水的作用是________________;
(2)实验二目的是验证铁生锈与![]() 有关,为了达到实验目的,应对b中实验做出的改进是______;
有关,为了达到实验目的,应对b中实验做出的改进是______;
(3)由实验三的现象可知,![]() 具有___________的性质;
具有___________的性质;
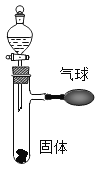
(4)在实验四中,要使热水中的白磷在水下燃烧,补充的实验是________________。
【答案】吸收五氧化二磷以免污染空气,吸收热量降温 水上面放一层植物油 不能燃烧、不能支持燃烧、密度比空气大 用导气管向热水中的白磷通氧气
【解析】
(1)实验一中水的可以吸收五氧化二磷以免污染空气,降温;
(2)实验二应对b中水上面放一层植物油,防止空气中氧气溶解与水;
(3)二氧化碳可以灭火,![]() 具有不能燃烧、不能支持燃烧、密度比空气大的性质;
具有不能燃烧、不能支持燃烧、密度比空气大的性质;
(4)根据燃烧条件可知,在实验四中,要使热水中的白磷在水下燃烧,还需要接触氧气。
(1)实验一中水的作用是吸收五氧化二磷以免污染空气,吸收热量降温;
(2)实验二目的是验证铁生锈与![]() 有关,为了达到实验目的,应对b中实验做出的改进是水上面放一层植物油,防止空气中氧气溶解与水;
有关,为了达到实验目的,应对b中实验做出的改进是水上面放一层植物油,防止空气中氧气溶解与水;
(3)由实验三的现象可知,![]() 具有不能燃烧、不能支持燃烧、密度比空气大的性质;
具有不能燃烧、不能支持燃烧、密度比空气大的性质;
(4)根据燃烧条件可知,在实验四中,要使热水中的白磷在水下燃烧,还需要接触氧气,补充的实验是用导气管向热水中的白磷通氧气。

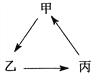
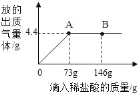
【题目】金属A和非金属B可直接合成化合物AB,甲、乙、丙三人分别做A和B化合反应的实验,充分反应时各人所用A和B的质量不同,但总质量都是9g。甲、乙所用A和B的质量及三人得到化合物AB的质量如下表,请填写表中的空格。
A的用量 | B的用量 | 得到的AB的质量 | |
甲 | 7g | 2g | 6g |
乙 | 4g | 5g | 6g |
丙 | __________ | _________ | 7.5g |
【题目】在一次化学实验中,同学们将饱和硫酸铜溶液逐滴加到5mL饱和氢氧化钠溶液中,观察到以下异常实验现象:
实验序号 | 滴加 | 实验现象 |
① | 第1~6滴 | 产生蓝色沉淀,但震荡后沉淀消失,形成亮蓝色溶液 |
② | 第7~9滴 | 产生蓝色沉淀,且沉淀逐渐增多,振荡后沉淀不消失,很快沉淀逐渐变黑色 |
实验①中蓝色沉淀为什么消失?同学们继续进行如下探究.
(查阅资料)
(1)氢氧化铜在室温下稳定,70℃-80℃时可脱水分解生成氧化铜
(2)铜酸钠![]() 溶于水,溶液呈亮蓝色
溶于水,溶液呈亮蓝色
(猜想与讨论)
小陶认为蓝色沉淀消失可能是氢氧化铜发生了分解.其地同学一致否定了他的猜测,理由是________________________________________。
同学们交流讨论后,提出以下两种猜想.
猜想一:少许氢氧化铜可溶于足量水中.
猜想二:氢氧化铜可在足量氢氧化钠浓溶液中溶解,溶液呈亮蓝色.
(实验探究)
为验证猜想,同学们用氢氧化铜粉末(其它试剂可任选)设计如下实验,请你填写表中的空格.
实验序号 | 实验方法与操作 | 实验现象 | 结论 |
③ | 将少许 5mL蒸馏水中,充分振荡 | ________________________ | 猜想一错误 |
④ | ________________________ | ________________________ | 猜想二正确 |
(结论与反思)
(1)根据实验,并进一步查阅资料知道,氢氧化铜在氢氧化钠溶液中溶解生成![]() ,反应的化学方程式是________________________________.
,反应的化学方程式是________________________________.
(2)根据实验可知饱和硫酸铜溶液与饱和氢氧化钠溶液的反应是放热反应,依据的实验现象________.