题目内容
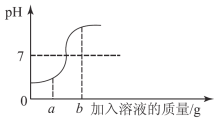
【题目】(5分)在用稀盐酸和氢氧化钠溶液进行中和反应实验时,反应过程中溶液的酸碱度变化如图所示。
(1)该反应的化学方程式为 。
(2)该实验操作是将 滴加到另一种溶液中。
(3)当加入溶液的质量为a g时,所得溶液中的溶质为 (写化学式)。
(4)当加入溶液的质量为b g时,向所得溶液中滴加酚酞溶液,溶液呈 色。
【答案】(1)HCl+NaOH==NaCl+H2O (2)氢氧化钠溶液 (3)NaCl HCl (4)红
【解析】
试题分析:(1)稀盐酸与氢氧化钠反应生成的是氯化钠和水;HCl+NaOH==NaCl+H2O;
(2)由反应的PH 变化可知,溶液的起始PH<7,说明是氢氧化钠滴入盐酸中;
(3)由图可知,当加入溶液的质量为a g时,所得溶液的PH<7,即酸过量,那么溶液中的溶质有:过量的盐酸和生成的氯化钠;
(4)当加入溶液的质量为b g时,溶液的PH>7,即溶液呈碱性,碱性溶液能使无色的酚酞试液变成红色。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目