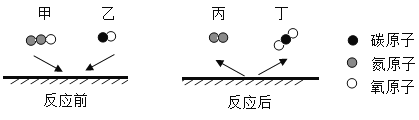
题目内容
【题目】某课外活动中,学生利用如图所示的杠杆完成探究实验,杠杆已调至平衡。
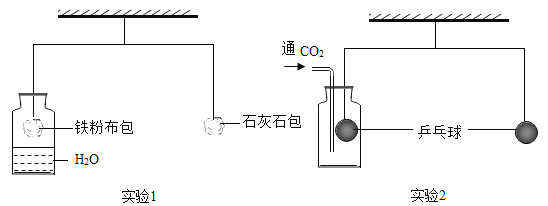
(1)实验1中,较长时间后,左边铁粉布包会____ (填“上升”或“下降”)下降,是因为铁粉与水、氧气发生了反应;
(2)将铁粉换成下列物质中的____ (填序号),杠杆也会出现相似现象。
A NaCl
B NaOH
C CaO
(3)实验2中,通入CO2一段时间,左边边乒乓球____ (填“上升”或“下降”);再往集气瓶中滴入足量NaOH溶液,杠杆重新平衡,其反应的化学方程式为___。
【答案】下降 BC 上升 CO2+2NaOH=Na2CO3+H2O
【解析】
(1)实验1中,较长时间后,左边铁粉布包下降,是因为铁粉与氧气、水发生了反应,生锈,质量增加; NaOH 、CaO均有吸水性,质量增加,也会出现下降的现象,故选BC;
(2)实验2中,通入CO2一段时间,由于二氧化碳的密度比空气的大,左边乒乓球受到的浮力增大,左边乒乓球上升,右边乒乓球下降,再往集气瓶中滴入足量NaOH溶液,二氧化碳和氢氧化钠反应生成碳酸钠和水,二氧化碳被吸收,杠杆重新平衡,发生反应的化学方程式为CO2+2NaOH=Na2CO3+H2O。

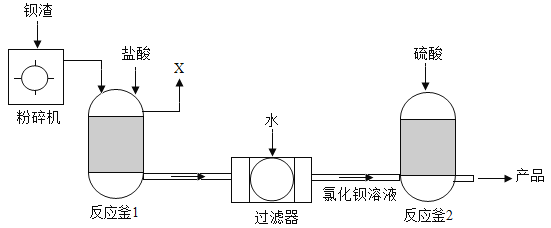
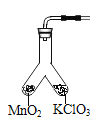
【题目】某学习小组利用如图所示装置对氯酸钾制氧气进行探究学习。

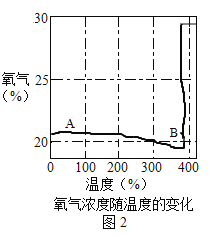
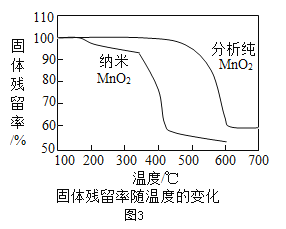
资料:①KClO3的熔点约为356℃,MnO2在加热条件下不分解;②KClO3分解时,传感器得到氧气浓度随温度的变化示意图及使用不同催化剂时的固体残留率分别如图和如图所示。
(1)由如图1可知,KClO3分解温度__________(填“高于”、“等于”或“低于”)其熔点。
(2)如图2中A→B段氧气浓度逐渐降低的可能原因是______________。
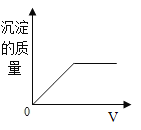
(3)分析如图3可知,对KClO3分解催化效果更好的催化剂是_____________。
(4)为证实MnO2的催化作用,小组同学利用如图装置进行如表所示的实验,请完成填表。
步骤 | 实验操作 | 实验现象 |
Ⅰ | 检查装置气密性 | (气密性良好) |
Ⅱ | 分别在“Y形管两支管中加入少量MnO2和KClO3,塞紧橡皮塞,用带火星木条放在导管口 | 没有_________ |
Ⅲ | 分别先后加热MnO2和KClO3,用带火星木条放在导管口,加热__________(填“左”或“右”)侧支管后,带火星木条复燃 | _________ |
Ⅳ | 冷却后,将"Y”形管左侧支管中部分MnO2混入右侧支管中,振荡“Y”形管,加热,用带火星木条放在导管口 | _________ |
(5)步骤Ⅳ的实验现象不能说明MnO2是KClO3分解的催化剂,因为还需要证明___________。
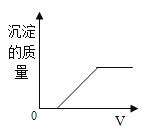
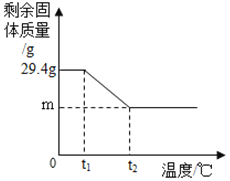
(6)将29.4gKC1O3和MnO2混合物以5:1配比加热至完全反应,如图中m的值应为_____g。
【题目】化学实践活动课上,老师拿来一包粉末。它是由长期放置在空气中的铁粉和久置的碱石灰干燥剂混合而成。让同学们设计实验进行探究。
[提出问题]固体样品的成分是什么?
[查阆资料] (1)碱石灰干燥剂是CaO和NaOH的混合物。
(2)BaCl2溶液是中性。
[猜想与假设]
固体样品中可能含有Fe、Fe2O3、 CaO、 NaOH、Ca(OH)2、Na2CO3和_________等七种物质。
[进行实验]如图
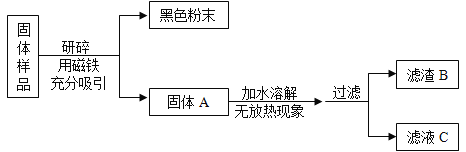
甲组同学对滤渣B的成分进行探究,记录如下:
实验操作 | 实验现象 | 实验结论及化学方程式 |
取少量滤渣B于试管中,加入足量稀盐酸,将生成的气体通入澄清的石灰水中 | ①____ ②_____ | 结论:滤渣B中有Fe2O3、CaCO3。实验操作中反应的化学方程式为:__ |
乙组同学对滤液C的成分进行了探究。记录如下:
实验操作 | 实验现象 | 实验结论 |
取少量滤液C于试管中,加入过量BaCl2溶液,静置,向上层清液中滴加无色酚酞试液,振荡 | ①有白色沉淀生成 ②酚酞试液由无色变成红色 | 滤液C中有___ |
[解释与结论]
(1)乙组同学实验中加入过量BaCl2溶液的目的是__________。
(2)通过以上实验探究。该固体样品中能确定一定含有的成分是_______。
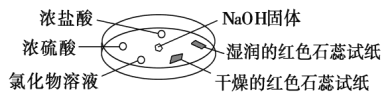
【题目】如图利用培养皿探究氨气的性质。实验时向NaOH固体上滴几滴浓氨水,将产生氨气。立即用另一表面皿扣在上面。下表中对实验现象所做的解释正确的是( )
选项 | 实验现象 | 解释 |
① | 浓盐酸附近产生白烟 | NH3与HCl反应生成了NH4Cl固体 |
② | 浓硫酸附近无明显现象 | NH3与浓硫酸不发生反应 |
③ | 氯化物溶液中有红褐色沉淀 | 该溶液一定有FeCl3溶液 |
④ | 干燥的红色石蕊试纸不变色,湿润的红色石蕊试纸变蓝 | NH3是一种可溶性碱 |
A.②③④
B.①③④
C.①③
D.③④