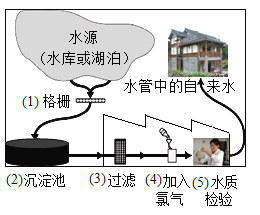
题目内容
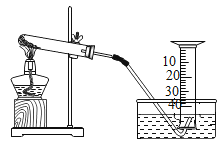
【题目】化学兴趣小组的同学利用如图所示的装置,对质量守恒定律进行探究。试回答下列问题。
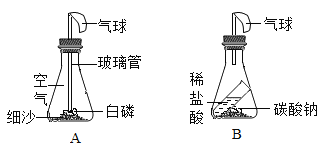
(1)I.提出问题:白磷在空气中燃烧遵循质量守恒定律吗?
Ⅱ.设计实验:小明同学将一定质量的白磷放入装置内,称得A装置的总质量为208.3g。然后将红热的玻璃管伸入瓶内,并立即塞紧橡胶塞。
Ⅲ.观察现象:此时观察到锥形瓶内的现象是_________,装置冷却后,再次称得A装置的总质量为208.3g。
Ⅳ.总结:①该反应遵循质量守恒定律。
②在实验设计上,玻璃管上方系一个瘪气球的目的是____________。
③实验结束后(锥形瓶已冷却至室温),发现瓶中白磷过量,为防止白磷在空气中燃烧,将锥形瓶瓶口倒置于盛满水的水槽中,拔下瓶塞,发现水进入锥形瓶中,则进入瓶中的水约占锥形瓶容积的________,原因是________。
(2)小兵同学认为碳酸钠与稀盐酸反应(化学方程式为NaCO3+2HC1=2NaCl+H2O+CO2↑)也遵循质量守恒定律。于是他设计了B装置,药品及装置的总质量为308.5g,反应结束后,他与小明的实验进行对比:冷却至室温,气球胀大的是_______(填“A”或“B”即或“A和B”);称量反应后药品及装置的总质量为308.3g,你认为小兵同学数据减少的原因可能是_____(填字母)。
A 稀盐酸不足
B 碳酸钠中含有不与稀盐酸反应的杂质
C 装置气密性不好
D 气球受到浮力的影响
(3)小结:由质量守恒定律可,化学反应前后一定不变的是________(填序号)。
①原子数目
②原子的种类
③分子数目
④分子的种类
⑤元素的种类
⑥物质的总质量
⑦物质的种类
(4)某登山运动员要登上最高峰一一珠程朗玛峰峰顶,需要自带氧气。假如每名运动员冲顶时消耗自带液氧4.8kg,若在实验室用高锰酸钾为原料制取相同质量的氧气,则需要高锰酸钾的质量为__________。
【答案】白磷燃烧,产生白烟,放出大量的热,气球胀大 平衡装置内外气压,防止瓶塞飞出 ![]() 白磷燃烧消耗了氧气,氧气约占空气总体积的
白磷燃烧消耗了氧气,氧气约占空气总体积的![]() B CD ①②⑤⑥ 47.4kg
B CD ①②⑤⑥ 47.4kg
【解析】
探究质量守恒定律进行探究,根据实验装置图可知:
(1)I、提出问题:白磷在空气中燃烧遵循质量守恒定律吗?
Ⅱ、设计实验:小明同学将一定质量的白磷放入装置内,称得A装置的总质量为208.3g。然后将红热的玻璃管伸入瓶内,并立即塞紧橡胶塞。
Ⅲ、观察现象:此时观察到锥形瓶内的现象是白磷燃烧,产生白烟,放出大量的热,气球胀大,装置冷却后,再次称得A装置的总质量为208.3g。

【题目】某兴趣小组对KClO3分解反应的催化剂进行研究,在相同的加热条件下,用下图装置完成表中实验:
编号 | KClO3质量/g | 催化剂 | 催化剂质量/g | 收集50mLO2所需时间/s |
实验1 | 5 | - | - | 171 |
实验2 | 5 | MnO2 | 0.5 | 49 |
实验3 | 5 | Fe2O3 | 0.5 | 58 |
实验4 | 5 | KCl | 0.5 | 154 |
(1)设置实验1的目的是________。
(2)表中所列3种催化剂的催化效果最佳的是________。
(3)写出KC1O3分解的化学方程式:________。
(4)由实验1和实验4可知,KCl有催化作用。维持加热条件不变,用实验1再继续收集收集50mLO2,所需时间明显少于171s,解释原因:___________。
(5)要比较KClO3分解反应中不同催化剂的催化效果,除了测量收集50mLO2所需时间外,还可以测量相同时间内_____________。
【题目】对比实验和控制变量法是化学中常用的探究问题和分析解决问题的科学方法。
(1)20℃时,某实验小组取不同质量的硝酸钾,分别加入到100g水中,充分溶解后,所得溶液的质量与加入硝酸钾的质量对应关系如表:
实验一 | 实验二 | 实验三 | 实验四 | |
硝酸押钾的质量/g | 20.0 | 25.0 | 30.0 | 35.0 |
所得溶液的质量/g | 120.0 | 125.0 | 130.0 | 131.6 |
①根据上表数据,实验二所得的溶液为____________(填“饱和溶液”或“不饱和溶液”)。
②若想要观察到实验四的35g硝酸钾全部溶解于水中,可采取的方法是__________。
(2)如图是氢分子和氧分子运动的示意图。
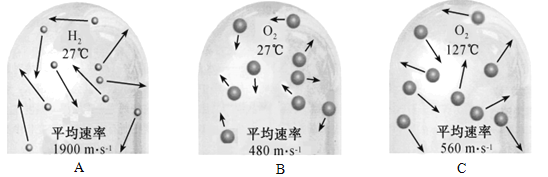
①在A、B和C中,能比较得出“温度越高,分子运动速率越快”的是__________(填字母序号)。
②从图中可见,影响分子运动速率的因素除温度外,还与__________有关。