题目内容
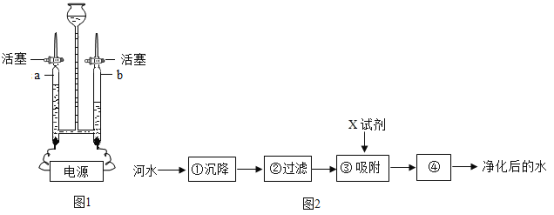
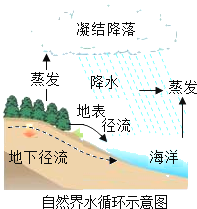
【题目】如图表示许昌市饮用水的净化过程,请回答下列问题:
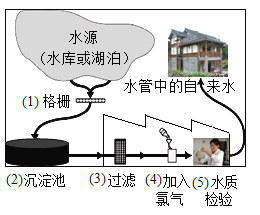
(1)地下水中的细菌和颗粒物等杂质比湖水、河水等地表水中的少,请说出一个原因____。
(2)在图中的沉淀池中,除了用静置的方法外,还可以用______的方法使水更干净。
(3)水质检验后,如果自来水在传输过程中存在细菌污染,人们在家中饮用该水之前应该如何处理?
_______________。
【答案】地下水经过了沙石、土壤等的过滤 加明矾形成胶状物质吸附杂质 加热煮沸,利用高温灭菌
【解析】
结合水的净化过程图可知:
(1)地下水中的细菌和颗粒物等杂质比湖水、河水等地表水中的少,可能的原因是地下水经过了沙石、土壤等的过滤。
(2)在图中的沉淀池中,除了用静置的方法外,还可以用加明矾形成胶状物质吸附杂质的方法使水更干净。
(3)水质检验后,如果自来水在传输过程中存在细菌污染,人们在家中饮用该水之前应该加热煮沸,利用高温进行灭菌。

练习册系列答案
相关题目