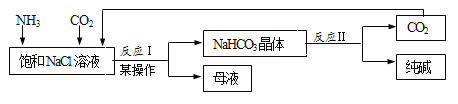
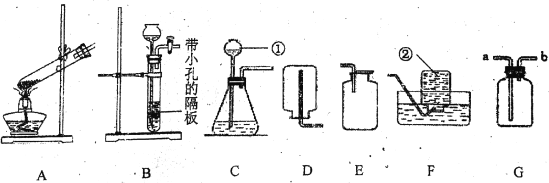
题目内容
【题目】下表是NaCl 、KClO3在不同温度下的溶解度(单位:g/100g水)。
温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 |
| 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| 3.3 | 7.3 | 13.9 | 23.8 | 37.5 | 56.3 |
(1) 20℃时,NaCl的溶解度为__________;40℃时,将20g KClO3放入100g水中,所得溶液溶质质量分数为__________(精确到0.1%)。
(2)“海水晒盐”利用的方法是________(填“蒸发结晶”或“降温结晶”);
(3)工业上用氯化钠溶液制备氯酸钾,主要流程如下:
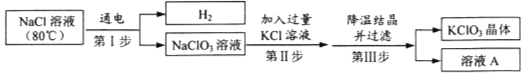
①上述流程中,氯化钠溶液中的水是否参与第I步化学反应?________(填“是”或“否”),你的判断依据是_______________________。
②写出第III步中发生反应的化学方程式_______________________。
③溶液A中的溶质除NaCl外,还含有________________(填化学式)。
【答案】 36.0g 12.2% 蒸发结晶 是 元素守恒 NaClO3+KCl=NaCl+KClO3 KCl、KClO3
【解析】根据所学知识和题中信息知,(1) 20℃时,NaCl的溶解度为36.0g。40℃时,氯酸钾溶解度为13.9g.将20g KClO3放入100g水中,所得溶液溶质质量分数为∶![]() ×100%=12.2%。(2)“海水晒盐”利用的方法是蒸发结晶. (3)工业上用氯化钠溶液制备氯酸钾. ①上述流程中,氯化钠溶液中的水是参与第I步化学反应。判断依据是元素守恒。②第III步中发生反应的化学方程式是NaClO3+KCl=NaCl+KClO3 。③溶液A中的溶质除NaCl外,还含有KCl、KClO3。
×100%=12.2%。(2)“海水晒盐”利用的方法是蒸发结晶. (3)工业上用氯化钠溶液制备氯酸钾. ①上述流程中,氯化钠溶液中的水是参与第I步化学反应。判断依据是元素守恒。②第III步中发生反应的化学方程式是NaClO3+KCl=NaCl+KClO3 。③溶液A中的溶质除NaCl外,还含有KCl、KClO3。
点睛∶本题主要考查溶解度,溶质质量分数,海水提纯,工业上用氯化钠溶液制备氯酸钾等知识。

【题目】某兴趣小组以“稀硫酸与氢氧化钠溶液能否发生反应”为课题进行了科学探究。如图1所示,小组同学向烧杯中的氢氧化钠溶液加入稀硫酸,一会儿会发现忘记了滴加指示剂,因此,他们停止滴加稀硫酸,并对烧杯内稀硫酸与氢氧化钠溶液是否发生了反应进行探究。

(1)小组同学设计了以下实验方案:
实验步骤 | 实验现象 | 实验结论 |
在白瓷板上放一小片pH试纸,用玻璃棒蘸取少量反应后的溶液滴在pH试纸上,把试纸显示的颜色与标准比色卡比较,读溶液的pH | pH 7 | 稀硫酸与氢氧化钠溶液发生了反应,且稀硫酸过量了 |
(2)写出该反应的化学方程式: 。
(3)同学们经过讨论一致认为,不用上述方法,用其他试剂也可以证明稀硫酸与氢氧化钠溶液能发生反应,于是分成甲、乙两组继续试验:
甲组实验:探究CuSO4溶液是否可以证明稀硫酸与氢氧化钠溶液发生反应。
【实验操作及现象】如图2,向a试管中滴加足量稀硫酸时无明显现象,再滴加CuSO4溶液时没有出现蓝色沉淀。
【实验结论】通过以上实验操作及现象,你认为用CuSO4溶液 (填“可以”或“不可以”)证明稀硫酸与氢氧化钠溶液能发生反应。
乙组实验:探究BaCl2溶液是否可以证明稀硫酸与氢氧化钠溶液发生反应。
【实验操作及现象】如图3,向b试管中滴加足量NaOH溶液时无明显现象,再滴加BaCl2溶液时出现白色沉淀。
【实验结论】通过以上实验操作及现象,你认为用BaCl2溶液 (填“可以”或“不可以”)证明稀硫酸与氢氧化钠溶液能发生反应,理由是 。
【题目】中国的茶具,除实用价值外,也有颇高的艺术价值。常用的茶具多为陶瓷或玻璃器皿。请从23-A、23-B两题中选一题作答,若两题均作答,以23-A题计分。
23-A | 23-B |
普通玻璃是Na2SiO3、CaSiO3、SiO2等物质经熔化后熔合在一起所得,玻璃是________(填“纯净物”或“混合物”);将纯碱、石英砂(SiO2)、石灰石等原料粉碎,按照适当的比例混合后,经过高温加热制得普通玻璃,同时会产生CO2。写出纯碱与石英砂发生反应的化学方程式_______。 | 紫砂茶具属于陶瓷器。紫砂是指矿石成分中二氧化硅、氧化铝及氧化铁含量较高的陶土。SiO2、Al2O3、Fe2O3都属于________(填“单质”或“氧化物”);某地紫砂中含氧化铝和氧化铁的质量分数分别为17%和3%。 请选择Al2O3、Fe2O3中的一种物质,计算该物质中所含各元素的质量比________。 |