题目内容
【题目】我国化工专家侯德榜创立了“侯氏制碱法”,促进了世界制碱技术的发展。流程简图如下(已知:母液中有一种铵态氮肥) ,下列有关说法不正确的是
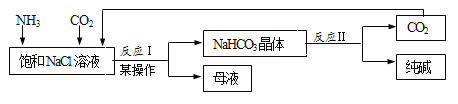
A. 反应中先通入氨气的目的是促进二氧化碳的吸收,提高产率
B. 流程中“某操作”用到的玻璃仪器有:玻璃棒、烧杯、量筒
C. 反应II得到的CO2可以循环使用
D. 反应I的方程式为NaCl+NH3+CO2=NaHCO3↓+NH4Cl
【答案】BD
【解析】根据氨气的水溶液显碱性考虑;
“某操作”很明显是固液分离,据此考虑实验仪器;
根据二氧化碳的性质考虑;
根据沉淀池发生的反应是氯化钠、氨气、二氧化碳和水,结合生成物进行考虑。
解:A. 氨气的水溶液显碱性,能更好的吸收二氧化碳,使反应物浓度增大,反应速度快,故正确;
B. “某操作”很明显是固液分离,应为过滤。所用玻璃仪器为:烧杯、漏斗、玻璃棒,故错误;
C.由图示可知,CO2可以循环使用,正确;
D.沉淀池发生的反应是氯化钠、氨气、二氧化碳和水,生成物是碳酸氢钠和氯化铵,反应的化学方程式为:NaCl+H2O+NH3+CO2=NaHCO3↓+NH4Cl,错误。
故本题选BD。

【题目】下表是NaCl、KNO3两种物质在不同温度时的溶解度,请回答下列问题:
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 |
NaCl的溶解度/g | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
KNO3的溶解度/g | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110.0 |
(1)上表中两种物质的溶解度受温度影响变化较大的是______;
(2)50℃时,KNO3的溶解度是____g;
(3)20℃时,取20g氯化钠放入50g水里,充分溶解后,可得到溶液的质量为____g;
(4)按照下图所示依次进行相关操作(每步均充分溶解),分别得到A、B、C三种溶液,其中属于不饱和溶液的是______(填字母序号),C溶液中溶质质量分数为_____(取整数)。

【题目】下表是NaCl 、KClO3在不同温度下的溶解度(单位:g/100g水)。
温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 |
| 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| 3.3 | 7.3 | 13.9 | 23.8 | 37.5 | 56.3 |
(1) 20℃时,NaCl的溶解度为__________;40℃时,将20g KClO3放入100g水中,所得溶液溶质质量分数为__________(精确到0.1%)。
(2)“海水晒盐”利用的方法是________(填“蒸发结晶”或“降温结晶”);
(3)工业上用氯化钠溶液制备氯酸钾,主要流程如下:
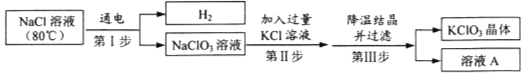
①上述流程中,氯化钠溶液中的水是否参与第I步化学反应?________(填“是”或“否”),你的判断依据是_______________________。
②写出第III步中发生反应的化学方程式_______________________。
③溶液A中的溶质除NaCl外,还含有________________(填化学式)。
