题目内容
【题目】人类社会的发展离不开金属,请依据所学知识填空。
(1)金属材料具有广泛的用途。我国大型C919客机大量使用了铝锂合金,钛合金等。其原因是合金比纯金属具有_____。在空气中,铝比铁具有更好的抗腐蚀性。原因是_____(用文字叙述).下列金属制品中,其用途利用金属导热性的是_____(填字母序号)

(2)金属资源在地球上分布广泛。人们在自然界中仅发现金、银等少数金属单质,其余金属元素都以化合物形式存在,你认为金属的存在形式主要和_____有关。农业上用硫酸铜,生石灰加水配制波尔多液作为杀菌剂,有经验的农民都不用铁制容器来配制或盛放波尔多液,原因是_____(用化学方程式表示),该反应类型为_____。
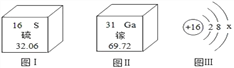
(3)某硫酸厂开采的黄铁矿(主要成分是FeS2)是生产H2SO4的重要原料。利用黄铁矿生产H2SO4的第一步反应为:4FeS2+11O2═2Fe2O3+8X.所得产物Fe2O3是冶炼铁的重要原料。已知FeS2中Fe的化合价为+2,则S的化合价为_____,X的化学式是_____,高炉中CO还原Fe2O3的化学方程式为_____。工业上用盐酸除铁锈的化学方程式为_____。
【答案】 更高的强度和更好的抗腐蚀性 铝与空气中的氧气反应生成致密的氧化膜对里面的金属起着保护作用 A 金属活动性强弱 Fe+CuSO4=Cu+FeSO4 置换反应 ﹣1 SO2 3CO+Fe2O3![]() 2Fe+3CO2 Fe2O3+6HCl=2FeCl3+3H2↑
2Fe+3CO2 Fe2O3+6HCl=2FeCl3+3H2↑
【解析】(1) 金属材料具有广泛的用途。我国大型C919客机大量使用了铝锂合金,钛合金等。其原因是合金比纯金属具有更高的强度和更好的抗腐蚀性更高的强度和更好的抗腐蚀性;在空气中,铝比铁具有更好的抗腐蚀性。原因是铝与空气中的氧气反应生成致密的氧化膜对里面的金属起着保护作用;铁锅利用了铁的导热性,铜导线利用了铜的导电性,钢丝绳利用了钢的延展性,黄金饰品利用了金的金属光泽,故选A;(2)金属的存在形式主要和金属活动性强弱有关;农业上用硫酸铜,生石灰加水配制波尔多液作为杀菌剂,有经验的农民都不用铁制容,器来配制或盛放波尔多液,原因是:Fe+CuSO4=Cu+FeSO4 ,属于置换反应;(3) 已知FeS2中Fe的化合价为+2,根据化合物中正负化合价的代数和为0,则S的化合价为-1价,根据反应前后原子的数目不变,反应前铁原子为4个,硫原子为8个,氧原子为22个,反应后铁原子为4个,硫原子为0个,氧原子为6个,X前面的系数为8,故X中应该含有一个硫原子和两个氧原子,故X的化学式是SO2,一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,化学反应方程式为:3CO+Fe2O3![]() 2Fe+3CO2;稀盐酸和氧化铁反应生成氯化铁和水,化学方程式为:Fe2O3+6HCl=2FeCl3+3H2O。
2Fe+3CO2;稀盐酸和氧化铁反应生成氯化铁和水,化学方程式为:Fe2O3+6HCl=2FeCl3+3H2O。

 名校课堂系列答案
名校课堂系列答案【题目】梅老师带领的化学兴趣小组在学习资料卡片“石笋和钟乳石的形成”时,发现难溶于水的CaCO3当遇到溶有CO2的水时,会发生反应:CaCO3+CO2+H2O= Ca(HCO3)2,反应生成的Ca(HCO3)2溶解性较大。联想到实验室检验CO2时,将气体通入澄清石灰水中能生成CaCO3。若长时间往澄清石灰水中通入CO2会产生什么样的现象呢?如果长时间向碱溶液中通入二氧化碳又会如何反应?小章和小丽决定用小烧杯盛装一定量的氢氧化钠溶液并不断通入二氧化碳气体进行探究。
【提出问题】
氢氧化钠溶液中通入二氧化碳一段时间后,溶液中会有什么溶质?
【查阅资料】
(1)通入少量的二氧化碳时,NaOH与CO2能反应的化学方程式_____________。
(2)通入过量的二氧化碳时,反应的化学方程式为Na2CO3+CO2+H2O= 2NaHCO3
(3)碳酸氢盐都能溶于水
(4)Na2CO3、NaHCO3的溶液呈碱性、BaCl2呈中性
【提出猜想】
(1)溶质有NaOH、Na2CO3; (2)溶质为Na2CO3;
(3)溶质是___________________(填化学式); (4)溶质全部是NaHCO3
【设计实验方案】
实验步骤 | 实验现象 | 实验结论 |
①用试管取少量小烧杯中反应后的溶液,滴加几滴________试液(填酸碱指示剂) | 溶液变红色 | 该溶液显碱性 |
②将小烧杯中反应后剩下的溶液进行称量,然后滴加过量的BaCl2溶液 | 有_________生成 | 猜想(4)不成立 |
③取步骤②静置后的上层清液, 滴入稀盐酸 | 有气泡冒出 | 猜想(1)和(2)不成立 |
【得出结论】猜想(3)成立
【讨论交流】
(1)小王同学提出实验步骤①是多余的。你认为该实验设计_______________(填“需要”或“不需要”),理由______________________。
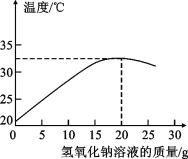
(2)将实验步骤②剩下混合物进行过滤、洗涤、干燥、称量。发现所得沉淀质量等于步骤②中所称量的溶液质量的十分之一,试计算氢氧化钠溶液中通入二氧化碳一段时间后,溶液中Na2CO3的质量分数为__________________。(写出计算过程,最后结果保留小数点后两位)
(3)验证二氧化碳性质时,如果长时间向澄清石灰水中通入二氧化碳会看到什么样的现象呢?请你描述一下:_____________________。
【知识拓展】
梅老师引导同学们再次研读教材,发现遇热或压强变小时,Ca(HCO3)2又能反应生成CaCO3,并告诉同学们,干粉灭火器中用NaHCO3灭火的原理与之类似,请写出该反应方程式_______,在生活中,NaHCO3还有许多用处,请说出一种____________。