题目内容
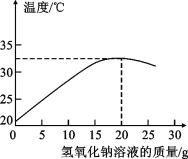
【题目】某化学兴趣小组的同学在实验室配制溶质质量分数为8%的氢氧化钠溶液,并用其测定某稀盐酸中溶质的质量分数。下图表示用该氢氧化钠溶液与10g某稀盐酸发生反应时溶液温度的变化情况。试计算稀盐酸中溶质的质量分数。
【答案】14.6%
【解析】
试题分析:由于中和反应放热,故随着反应的进行,溶液的温度逐渐升高,直至反应恰好完全,溶液温度达到最高,故根据图示可判断,当加入氢氧化钠那溶液的质量为20g时 ,反应恰好完全
解:分析图知与10g稀盐酸恰好完全反应的氢氧化钠质量为:20g×8%=1.6g
设稀盐酸中溶质的质量为x
NaOH+HCl=NaCl+H2O
40 36.5
1.6g x
40:1.6g=36.5:x
x=1.46g
稀盐酸中溶质的质量分数为:1.46g/10g=14.6%
答:稀盐酸中溶质的质量分数为14.6%

练习册系列答案
相关题目